
题目列表(包括答案和解析)
A.混合后,甲、乙溶液中的溶质的质量分数均大于5%
B.混合后,甲、乙溶液中溶质的质量分数均等于5%
C.混合后,甲溶液溶质的质量分数大于5%,乙溶液溶质的质量分数小于5%
D.混合后,甲溶液溶质的质量分数小于5%,乙溶液溶质的质量分数在于5%
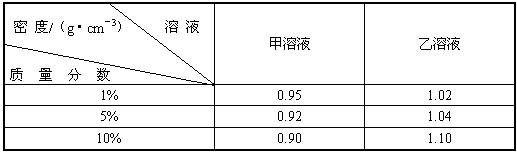
甲物质的溶质质量分数为1%溶液与9%溶液等体积混和,乙物质的溶质质量分数为1%溶液与9%溶液等体积混合,根据表中数据判断下列叙述正确的是( )

A.混合后,甲、乙溶液中的溶质的质量分数均大于5%
B.混合后,甲、乙溶液中溶质的质量分数均等于5%
C.混合后,甲溶液溶质的质量分数大于5%,乙溶液溶质的质量分数小于5%
D.混合后,甲溶液溶质的质量分数小于5%,乙溶液溶质的质量分数在于5%
| 溶解度(S)/g | 溶度积(Ksp) | 摩尔质量(M)/g?mol-1 | |||
| Ca(OH)2 | Ba(OH)2 | CaCO3 | BaCO3 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9×10-9 | 2.6×10-9 | 100 | 197 |
| 实验编号 | HA物质的量浓度 (mol?L-1) |
NaOH物质的量浓度 (mol?L-1) |
混合溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | c | 0.2 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=9 |
| 实验编号 | HA物质的量浓度(mol?L-1) | NaOH物质的量浓度(mol?L-1) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | c1 | 0.2 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=9 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com