
题目列表(包括答案和解析)
| 发展阶段 | 主要化学家 | 主要贡献 |
| (1) | 道尔顿(Dalton) | 近代原子论 近代原子论 |
| (2) | 汤姆逊 汤姆逊 |
葡萄干面包模型 |
| (3) | 卢瑟福(Rutherford) | 原子结构的行星模型 原子结构的行星模型 |
| (4) | 波尔(Bohr) | 现代原子论 |
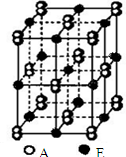 A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F.A原子核外电子分处三个不同能级,且每个能级上排布的电子数相同;C原子p轨道上成对电子数等于未成对电子数;D是电负性最大的元素;E原子是元素周期表上第一个4S能级有两个电子的原子;F的核外电子数等于A、B、C、D的电子数之和.请根据以上信息,回答下列问题:(答题时,A、B、C、D、E、F用所对应的元素符号表示)
A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F.A原子核外电子分处三个不同能级,且每个能级上排布的电子数相同;C原子p轨道上成对电子数等于未成对电子数;D是电负性最大的元素;E原子是元素周期表上第一个4S能级有两个电子的原子;F的核外电子数等于A、B、C、D的电子数之和.请根据以上信息,回答下列问题:(答题时,A、B、C、D、E、F用所对应的元素符号表示)| 氟化物 | G的氟化物 | Q的氟化物 | R的氟化物 | 熔点/K | 993 | 1539 | 183 |


| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com