
题目列表(包括答案和解析)
| 1 |
| 2 |
| (x-0.04y) |
| 0.06 |
| 1 |
| 2 |
| (x-0.04y) |
| 0.06 |
| ||
| ||
| C(CH3OH)C(H2O) |
| C(CO2)C3(H2) |
| C(CH3OH)C(H2O) |
| C(CO2)C3(H2) |
| 容 器 | 甲 | 乙 |
| 反应物 投入量 |
1molCO2 3molH2 |
a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) |

研究碳及其化合物的综合利用对促进低碳社会的构建具有重要的意义。请运用相关知识研究碳及其化合物的性质。
(1)近年来,我国用电弧法合成的碳纳米管中常伴有大量碳纳米颗粒(杂质),这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式为:
?? C+?? K2Cr2O7+ ?????? —?? ?? CO2↑+ ?? K2SO4 + ?? Cr2(SO4)3+?? H2O
①完成并配平上述化学方程式。
②在上述方程式上用单线桥标出该反应电子转移的方向与数目。
(2)高温时,用CO还原MgSO4可制备高纯MgO。
①750℃时,测得气体中含等物质的量SO2和SO3,此时反应的化学方程式是?????????????????? 。
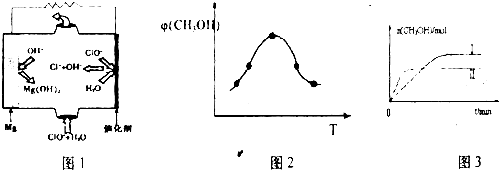
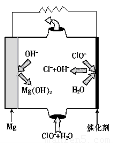
②由MgO可制成“镁-次氯酸盐”电池,其装置示意图如图1,该电池反应的离子方程式为 ????????? 。
 ????
????  ??
??  ?
?
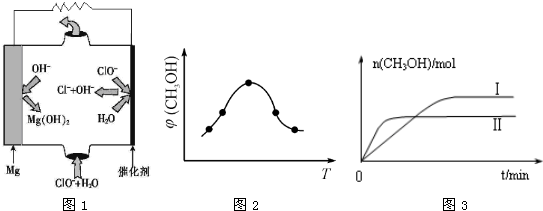
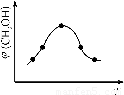
图1????????????????? 图2????????????????? 图3
(3)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:CO2(g) +3H2(g) CH3OH(g) +H2O(g)? △H
CH3OH(g) +H2O(g)? △H
①该反应的平衡常数表达式为K=???? ????? ????? 。
②取五份等体积CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图2所示,则上述CO2转化为甲醇反应的△H?????? 0(填“>”“<”或“=”)。
③在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图3所示,曲线I、II对应的平衡常数大小关系为KⅠ????? KII(填“>” “<”或“=”)。
下图是部分常见元素的单质及其化合物的转化关系图(有关反应的条件及生成的部分产物已略去)。已知:E为红棕色固体,K为浅绿色溶液;反应①②是化工生产中的重要反应;B、C、D、H是单质;B、C、D、F、G、H常温下是气态; F和H的水溶液均具有漂白作用,且F是形成酸雨的主要物质之一;N是一种常见的氮肥;化合物G为极易溶于水且易液化.
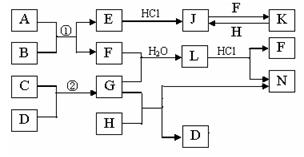
(1)化合物A中含有的短周期元素是 (写元素符号),E的化学式_______。
(2)如何检验化合物N中的阳离子 。
(3)写出J与F反应的离子方程式: ,G与H反应的化学方程式: 。
(4)等物质的量F和H的混合气体通入品红溶液中的现象为 ,原因是(用化学反应方程式表示) 。
(5)已知C与D反应生成1.7g G 时放出4.26kJ的热量,则该反应的热化学方程为
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com