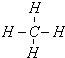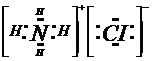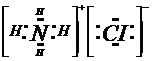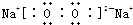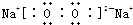短周期主族元素A、B、C、D、E、F的原子序数依次增大,它们的原子核外电子层数之和为13.已知B元素形成的化合物种类最多,D元素原子最外层电子数是次外层电子数的3倍,元素E的原子半径在同周期中最大,F元素原子最外层电子数等于其电子层数.
(1)C元素在元素周期表中的位置是
第二周期第ⅤA族
第二周期第ⅤA族
,B的单质与C的最高价氧化物对应水化物的浓溶液发生反应的化学方程式是
C+4HNO
3(浓)
CO
2↑+4NO
2↑+2H
2O
C+4HNO
3(浓)
CO
2↑+4NO
2↑+2H
2O
(2)由A、B、D、E四种元素形成的化合物中所含的化学键类型是
离子键、共价键
离子键、共价键
(3)写出E
2D
2与A
2D反应的离子方程式
2Na2O2+2H2O=4Na++4OH-+O2↑
2Na2O2+2H2O=4Na++4OH-+O2↑
.
(4)实验室配制100mL0.2mol?L
-1由A、D、E形成化合物的溶液,需要用到的玻璃仪器除烧杯、小烧杯外还有
100mL容量瓶、玻璃棒、胶头滴管
100mL容量瓶、玻璃棒、胶头滴管
;如果定容时仰视刻度线,则所配制溶液浓度
<
<
0.2mol?L
-1(埴“>”、“<”或“=”).将F的单质溶于上述配制的溶液中所发生反应的离子方程式是
2Al+2OH-+2H2O=+2AlO2-+3H2↑
2Al+2OH-+2H2O=+2AlO2-+3H2↑
.