
题目列表(包括答案和解析)
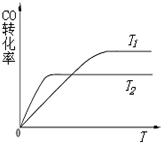 甲醇具有开发和应用广阔的前景.工业上一般采用下列两种途径合成甲醇:
甲醇具有开发和应用广阔的前景.工业上一般采用下列两种途径合成甲醇:| 温度 | 250℃ | 350℃ |
| K | 2.041 | 0.012 |
纳米氧化镁具有特殊的热、光、电、力学和化学等性能,有广泛的应用前景。下图是利用海水制盐的副产品制备纳米氧化镁的流程图。

(1)操作I包括蒸发结晶、____________。
(2)操作I后得到的母液中镁离子浓度为1.8×10-3 mol·L-1,要使镁离子产生沉淀,溶液的pH最低应为_____________。(已知:Ksp[Mg(OH)2]= 1.8×10-11)
(3)反应I中CO(NH2)2与H2O反应生成CO2和NH3·H2O,还发生另一主要化学反应的离子方程式为______________________________。
(4)某科研小组研究反应I在378K~398K时的反应时问、反应物的物质的量配比等因素对制备纳米氧化镁产率的影响。请完成以下实验设计表:
|
实验 编号 |
T/K |
反应 时间/h |
反应物的物质的量配比 n[CO(NH2)2]∶n[MgCl2•6H2O] |
实验目的 |
|
① |
378 |
3 |
3∶1 |
(I)实验①和③探究探究反应物的物质的量配比对产率的影响; (II)实验②和④探究 ; (III)实验②和 探究反应时间对产 率的影响。 |
|
② |
378 |
4 |
4∶1 |
|
|
③ |
378 |
3 |
|
|
|
④ |
398 |
4 |
4∶1 |
(5)下图为反应的温度对纳米MgO产率的影响。请归纳出温度对纳米MgO产率的影响规律________________________________。

某课外活动小组同学用右图装置进行相关的实验,试回答下列问题。

(1)若开始时开关K与a连接,则A极的电极反应式为 。
(2)若开始时开关K与b连接,则总反应的离子方程式为 。在该实验中,下列说法正确的是(填序号) 。
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润KI淀粉试纸变蓝
③反应一段时间后(设NaCl足量)加适量盐酸可恢复到电解前电解质的浓度
④若标准状况下B极产生2.24 L气体,则有0.2 mol电子转移
(3)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是 。
A.C(s) + H2O(g) =" CO(g)" + H2(g) △H > 0
B.NaOH(aq) + HC1(aq) =" NaC1(aq)" + H2O(1) △H < 0
C.2H2(g) + O2(g) = 2H2O(1) △H<0
(4)电解原理在化学工业中有着广泛的应用。右图中,a为电解液,X和Y是两块电极板,回答下列问题:

(4)①若X和Y均为惰性电极,a为CuSO4溶液,则电解时的化学反应方程式为 。通过一段时间后,向所得溶液中加入8g CuO粉末,恰好恢复电解前的浓度和pH,则电解过程中转移的电子的物质的量为 。
②若X、Y分别为铁和铜,a仍为CuSO4溶液,则Y极的电极反应式为 。
SO2是引起大气污染的主要有害气体之一,我国大气质量标准中规定大气中SO2的最高浓度限值如下表:大气中SO2三级标准浓度限值
| 浓度限值[mg/(m3空气)] | |||
| 一级标准 | 二级标准 | 三级标准 | |
| 年日平均 | 0.02 | 0.06 | 0.10 |
| 日平均 | 0.05 | 0.15 | 0.25 |
| 任何一次 | 0.15 | 0.50 | 0.70 |
注:“年日平均”为任何一年的平均浓度均值不许超过的限值;“日平均”为任何一日的平均浓度不许超过的限值;“任何一次”为任何一次采样测定不许超过的浓度限值。
据报道,1952年2月,某城市雾大无风,家庭和工厂排出的烟雾经久不散,大气中SO2的含量高达3.8mg/(m3空气) ,烟尘达4.5mg/(m3空气),居民健康普遍受到危害,4天之内死亡人数约4000,流经该城市的主要河道也因此而受到污染,引起鱼类死亡。大气中的SO2将直接危害陆生高等植物的____组织,大气中SO2超标最容易影响人的_______系统而患疾病,而河流中鱼类死亡与SO2造成大气污染所形成______有关。
某空气污染监测仪是根据SO2和Br2水的定量反应来测定空气中的SO2含量的。反应的溴来自一个装有酸性(稀硫酸)的KBr溶液的电解池阳极的氧化反应,电解池的阳极室与阴极室是隔开的。当测量某地区空气中SO2的含量时,一天中作了三次取样监测,每次取样的空气(已除尘)都以1.5×10-4m3.min-1的流速进入电解池的阳极室,从电流计显示出每次的电流强度分别为8.56×10-6A、9.25×10-6A 、8.12×10-6A,每次都能够保持电解池中Br2浓度恒定并恰好与二氧化硫完全反应(设空气中不含与溴反应的其它杂质、1个电子电量为1.6×10-19C)。
写出此监测过程中发生反应的化学方程式。计算该地区空气中二氧化硫的含量有没有达到大气质量标准?
当大气中SO2污染较严重时,目前有一种降低其危害的方法是用直升飞机喷撒白垩粉,其化学方程式为___________________。
某火力发电厂所在地有较丰富的碳酸钙矿和菱镁矿,若该发电厂以含硫重油作燃料,请就地取材提出三种化学反应原理与上一小题不同的“脱硫”方法(用化学方程式表示,):
第一种______________;第二种______________; 第三种______________。
某10 6 kW火力发电厂以重油为燃料。以含硫3.5%的重油为燃料,重油使用量为0.18 dm3.kW-1.h-1(重油的密度为0.95g.cm3)。该厂开工率(每年实际运转天数)为80%,对烟道气的脱硫效率为90%。问一年间对烟道气脱硫回收的SO2能生成多少吨石膏(CaSO4·2H2O)?
铁是地壳中含量第二的金属元素,其单质、合金及化合物在生产生活中的应用广泛。
(―)工业废水中含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的危害,必须进行处理。常用的处理方法是电解法,该法用Fe作电极电解含Cr2O72-的酸性废水,随着电解的进行,阴极附近溶液pH升高,产生Cr(OH)3沉淀。
(1)用Fe作电极的目的是 。
(2)阴极附近溶液pH升高的原因是_ (用电极反应式解释);溶液中同时生成的沉淀还有 。
(二)氮化铁磁粉是一种磁记录材料,利用氨气在400℃以上分解得到的氮原子渗透到高纯铁粉中可制备氮化铁。制备高纯铁粉涉及的主要生产流程如下:
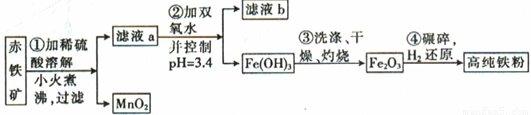
已知①某赤铁矿石含60.0%Fe2O3、3.6%FeO,还含有Al2O3、MnO2、CuO等。
②部分阳离子以氢氧化物形式完全沉淀时溶液的pH如下:

(3)步骤②中加双氧水的目的是
,pH控制在3.4的作用是
,已知25℃时,Ksp[Cu(OH)2] =2.0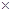 10-20,该温度下反应:Cu2++2H2O
10-20,该温度下反应:Cu2++2H2O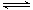 Cu(OH)2+2H+的平衡常数K=
。
Cu(OH)2+2H+的平衡常数K=
。
(4)如何判断步骤③中沉淀是否洗涤干净? 。
(5)制备氮化铁磁粉的反应:Fe+NH3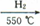 FexNy+H2 (未配平),若整个过程中消耗氨气34.0g,消耗赤铁矿石2 kg,设整个过程中无损耗,则FexNy磁粉的化学式为
。
FexNy+H2 (未配平),若整个过程中消耗氨气34.0g,消耗赤铁矿石2 kg,设整个过程中无损耗,则FexNy磁粉的化学式为
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com