
题目列表(包括答案和解析)
(6分)A、B、C、D四种短周期元素,原子序数D>C>B>A,且B、C、D同周期,A、D同主族,B 原子的最外层只有一个电子,C的原子结构示意图
为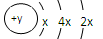 ,D在同周期元素中原子半径最小,据此填空:
,D在同周期元素中原子半径最小,据此填空:
(1)C元素的名称为 ,其气态氢化物的化学式为
(2)D在周期表的 周期, 族。
(3)A、B、C、D四种元素的原子半径由大到小的顺序为(用元素符号填写)
(4)B的最高价氧化物的水化物的化学式为
(6分)A、B、C、D四种短周期元素,原子序数D>C>B>A,且B、C、D同周期,A、D同主族,B 原子的最外层只有一个电子,C的原子结构示意图
为  ,D在同周期元素中原子半径最小,据此填空:
,D在同周期元素中原子半径最小,据此填空:
(1)C元素的名称为 ,其气态氢化物的化学式为
(2)D在周期表的 周期, 族。
(3)A、B、C、D四种元素的原子半径由大到小的顺序为(用元素符号填写)
(4)B的最高价氧化物的水化物的化学式为
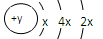 ,D在同周期元素中原子半径最小,据此填空:
,D在同周期元素中原子半径最小,据此填空:(6分)A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B同周期,C、D同主族,A的原子结构示意图为:  ,B、C可形成离子化合物
,B、C可形成离子化合物![]() ,据此填空:
,据此填空:
(1)A的元素名称为 ,其气态氧化物的化学式为 。
(2)A、B、C、D四种元索的原予,半径由小到大的顺序为 。
(3)B和C最高价氧化物的水化物化学式分别为 和 。
 2BO3(g);△H=-196.6kJ?mol-1
2BO3(g);△H=-196.6kJ?mol-1 2NGH3(g);△H=-92.4kJ/mol
2NGH3(g);△H=-92.4kJ/mol
| 4 |
| a2 |
| 4 |
| a2 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com