A、B、C、D四种短周期元素,A、B、C同周期,A的原子半径是同周期中最大的;B、D同主族.己知D元素的一种单质是日常生活中饮水机常用的消毒剂,C元素的单质可以从A、B两元素组成的化合物的水溶液中置换出B元素的单质.
(1)C元素在周期表中的位置
第三周期,第VIIA族
第三周期,第VIIA族
.
(2)A元素与水反应的离子方程式是
2Na+2H2O=2Na++2OH-+H2↑
2Na+2H2O=2Na++2OH-+H2↑
.
(3)写出C元素的单质从A、B两元素组成的化合物的水溶液中置换出B元素的单质的化学方程式
Cl2+Na2S=2NaCl+S↓
Cl2+Na2S=2NaCl+S↓
.
(4)BD
2和C
2均具有漂白性,二者的漂白原理
不同
不同
.(填“相同”或“不同”)
(5)B元素的单质在不同的条件下可以与O
2发生一系列反应:
B(s)+O
2=BO
2(g);△H=-296.8kj?mol
-12BD
2(s)+O
2(g)

2BO
3(g);△H=-196.6kJ?mol
-1则1mol BO
3(g)若完全分解成B(s),反应过程中的热效应为
△H=+395.1kJ/mol
△H=+395.1kJ/mol
.
(6)氢氧燃料电池能量转化率高,具有广阔的发展前景.如图(1)所示,电池中正极的电极反应式为
O2+2H20+4e-=4OH-
O2+2H20+4e-=4OH-
.
(7)氢气是合成氨的重要原料,合成氨反应的热化学方程式如下:
N
2(g)+3H
2(g)

2NGH
3(g);△H=-92.4kJ/mol

①当合成氨反应达到平衡后,改变某一外界条件(不改变N
2、H
2和NH
3的量),反应速率与时间的关系如图(2)所示.图中t
1时引起平衡移动的条件可能是
加压
加压
.其中表示平衡混合物中NH
3的含量最高的一段时间是
t2-t3
t2-t3
.
②温度为T℃时,将2a molH
2和a molN
2放入0.5L密闭容器中,充分反应后测得N
2的转化率为50%.则该反应的平衡常数为
.

 2BO3(g);△H=-196.6kJ?mol-1
2BO3(g);△H=-196.6kJ?mol-1 2NGH3(g);△H=-92.4kJ/mol
2NGH3(g);△H=-92.4kJ/mol
 2SO3(g);△H=-196.6kJ?mol-1,
2SO3(g);△H=-196.6kJ?mol-1, 2SO2(s)+O2(g);△H=+196.6kJ?mol-1,
2SO2(s)+O2(g);△H=+196.6kJ?mol-1,



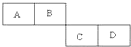 A、B、C、D四种短周期元素在周期表中的相对位置如表所示,A的单质与水蒸气反应可以制取水煤气.
A、B、C、D四种短周期元素在周期表中的相对位置如表所示,A的单质与水蒸气反应可以制取水煤气.