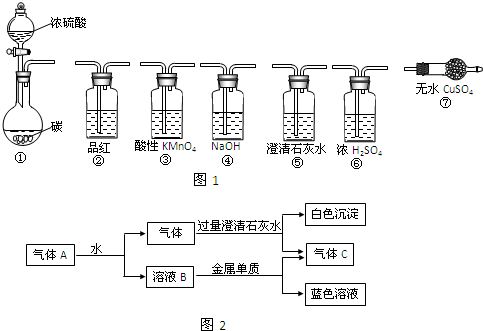
为探究乙烯与溴的加成反应,甲同学设计并进行了如下实验,将乙醇与浓硫酸的混合液加热至170℃,将生成的气体通入溴水中,发现溴水褪色,即证明乙烯与溴水发生了加成反应.
(1)写出甲同学实验中两个主要的化学方程式
;
CH2=CH2+Br2→CH2BrCH2Br
CH2=CH2+Br2→CH2BrCH2Br
.
(2)乙同学在甲同学的实验中发现,生成的气体有刺激性气味,推测产生的气体除乙烯外,还有副产物SO
2 和CO
2,SO
2也能使溴水褪色:SO
2+Br
2+2H
2O→H
2SO
4+2HBr
于是对甲同学的结论提出质疑.为确认乙烯能使溴水褪色,甲同学在实验时先将混合气体通过足量的
B
B
(填序号)以除去其中的SO
2,再通入溴水时发现剩余气体仍能使溴水褪色.
(A)氯水 (B)NaOH溶液 (C)酸性KMnO
4溶液
(3)乙同学又提出质疑,认为乙烯使溴水褪色也可能发生了取代反应:CH
2=CH
2+Br
2→CH
2=CHBr+HBr
甲同学认为很有道理,于是又做了一个简单的实验来确认是否发生取代反应,该实验所用的试剂是
紫色石蕊试液
紫色石蕊试液
,可能的现象和结论是
向反应后的溶液中滴加紫色石蕊试液,溶液不变红,说明该反应为加成反应而非取代反应,
向反应后的溶液中滴加紫色石蕊试液,溶液不变红,说明该反应为加成反应而非取代反应,
.

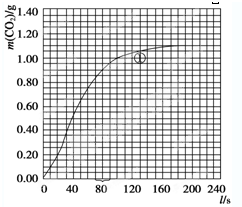
 (2012?闸北区一模)碳酸钠和碳酸氢钠在生产、生活中都有重要的应用.现有3.58g Na2CO3和NaHCO3固体混合物,将其制成溶液后,边搅拌边逐滴滴加80.0mL 1.0mol/L盐酸,反应完全后生成的CO2气体折算成标准状况下的体积为896mL(设气体全部逸出,下同).(1)通过计算可知上述反应中
(2012?闸北区一模)碳酸钠和碳酸氢钠在生产、生活中都有重要的应用.现有3.58g Na2CO3和NaHCO3固体混合物,将其制成溶液后,边搅拌边逐滴滴加80.0mL 1.0mol/L盐酸,反应完全后生成的CO2气体折算成标准状况下的体积为896mL(设气体全部逸出,下同).(1)通过计算可知上述反应中