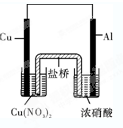
盐酸、硫酸和硝酸是中学阶段所常见的“三大酸”.现请就三大酸与金属铜反应情况,填空回答下列问题:
(1)我们知道,稀盐酸不与Cu反应.在稀盐酸中加入H
2O
2后,则可使铜顺利溶解.该反应的化学方程式为
Cu+H2O2+2HCl=CuCl2+2H2O
Cu+H2O2+2HCl=CuCl2+2H2O
;
(2)在一定体积的18mol/L的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9mol.则浓硫酸的实际体积
大于
大于
(填写“大于”、“等于”或“小于”)100mL.若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO
3溶液),则该反应的离子方程式为
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
;
(3)分别将等质量的铜片与等体积均过量的浓硝酸、稀硝酸反应,所得到的溶液前者呈绿色,后者呈蓝色,某同学提出这可能是Cu
2+浓度差异引起的,你同意这种看法吗?
不同意
不同意
(填“同意”或“不同意”),原因是
等质量的铜片与等体积、过量的浓硝酸、稀硝酸反应,所得溶液中Cu2+的浓度基本相等
等质量的铜片与等体积、过量的浓硝酸、稀硝酸反应,所得溶液中Cu2+的浓度基本相等
.另一同学提出溶液呈“绿色”是溶液中Cu
2+与NO
2共存的结果,请你设计实验探究此说法正确与否(简述实验方案和实验现象及由此得出的结论)
将一定量的
NO2通入铜片与稀硝酸反应后的溶液中,若溶液呈绿色,则该同学的结论正确,反之,不正确
将一定量的
NO2通入铜片与稀硝酸反应后的溶液中,若溶液呈绿色,则该同学的结论正确,反之,不正确
.



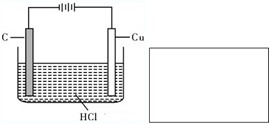 盐酸、硫酸和硝酸是中学常见的三种酸.
盐酸、硫酸和硝酸是中学常见的三种酸.