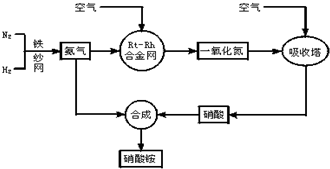
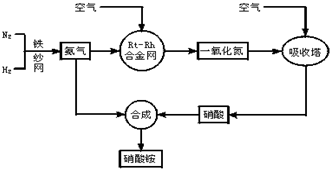
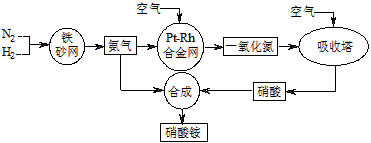
£Ø2009?ÉĻŗ£Ņ»Ä££©¹¤ŅµÉś²śĻõĖįļ§µÄĮ÷³ĢĶ¼ČēĶ¼£ŗ

Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Š“³öĻõĖįļ§ŌŚ¹¤Å©ŅµÉś²śÖŠµÄÖŲŅŖ×÷ÓĆ
æÉ×öµŖ·ŹµČ
æÉ×öµŖ·ŹµČ
£ØČĪŠ“Ņ»Ģõ£©
£Ø2£©ŅŃÖŖN
2£Øg£©+3H
2£Øg£©ØT2NH
3£Øg£©£¬”÷H=-92kJ?mol
-1£®Ēė»Ų“š£ŗ
¢ŁŌŚ500”ę”¢200atmŗĶĢś“ß»ÆĢõ¼žĻĀĻņŅ»ĆܱÕČŻĘ÷ÖŠ³äČė1molN
2ŗĶ3molH
2£¬³ä·Ö·“Ó¦ŗ󣬷ųöµÄČČĮæ
£¼
£¼
£ØĢī”°£¼”±”°£¾”±”°=”±£©92.4kJ£¬ĄķÓÉŹĒ
ŌŚ1atmŗĶ298KĢõ¼žĻĀ£¬1molµŖĘųŗĶ3molĒāĘųĶźČ«·“Ӧɜ³É2mol°±Ęų£¬·Å³ö92.4kJČČĮ棬øĆ·“Ó¦ĪŖæÉÄę·“Ó¦£¬²»æÉÄܽųŠŠĶźČ«£¬ÓÖŅņĪŖ·“Ó¦ĪĀ¶ČĪŖ500”ę£¬ĖłŅŌ·Å³öµÄČČĮæŠ”ÓŚ92.4kJ
ŌŚ1atmŗĶ298KĢõ¼žĻĀ£¬1molµŖĘųŗĶ3molĒāĘųĶźČ«·“Ӧɜ³É2mol°±Ęų£¬·Å³ö92.4kJČČĮ棬øĆ·“Ó¦ĪŖæÉÄę·“Ó¦£¬²»æÉÄܽųŠŠĶźČ«£¬ÓÖŅņĪŖ·“Ó¦ĪĀ¶ČĪŖ500”ę£¬ĖłŅŌ·Å³öµÄČČĮæŠ”ÓŚ92.4kJ
£®
¢ŚĪŖÓŠŠ§ĢįøßĒāĘųµÄ×Ŗ»ÆĀŹ£¬Źµ¼ŹÉś²śÖŠŅĖ²ÉČ”µÄ“ėŹ©ÓŠ
CEF
CEF
A£®½µµĶĪĀ¶Č B£®×īŹŹŗĻ“߻ƼĮ»īŠŌµÄŹŹµ±øßĪĀ C£®Ōö“óŃ¹Ēæ
D£®½µµĶŃ¹Ēæ E£®Ń»·ĄūÓĆŗĶ²»¶Ļ²¹³äµŖĘų F£®¼°Ź±ŅĘ³ö°±
£Ø3£©ŅŃÖŖ²¬īīŗĻ½šĶųĪ“Ō¤ČČŅ²»į·¢ČČ£®Š“³ö°±“ß»ÆŃõ»ÆµÄ»Æѧ·½³ĢŹ½£ŗ
£¬øĆ·“Ó¦µÄ»ÆŃ§Ę½ŗā³£Źż±ķ“ļŹ½K=
| C4(NO)?C6(H2O) |
| C4(NH3)?C5(O2) |
| C4(NO)?C6(H2O) |
| C4(NH3)?C5(O2) |
£¬µ±ĪĀ¶ČÉżøߏ±£¬KÖµ
¼õŠ”
¼õŠ”
£ØŌö“󔢼õŠ””¢ĪŽÓ°Ļģ£©£¬ĘäŌŅņŹĒ
ŅņĪŖ°±µÄ“ß»ÆŃõ»Æ·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬ĖłŅŌÉżøßĪĀ¶Č£¬K»į¼õŠ”£®
ŅņĪŖ°±µÄ“ß»ÆŃõ»Æ·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬ĖłŅŌÉżøßĪĀ¶Č£¬K»į¼õŠ”£®
£®
£Ø4£©ŌŚŅ»¶ØĪĀ¶ČŗĶŃ¹ĒæµÄĆܱÕČŻĘ÷ÖŠ£¬½«Ę½¾łŹ½ĮæĪŖ8.5µÄH
2ŗĶN
2»ģŗĻ£¬µ±øĆ·“Ó¦“ļµ½Ę½ŗāŹ±£¬²ā³öĘ½ŗā»ģŗĻĘųµÄĘ½¾łŹ½ĮæĪŖ10£¬“ĖŹ±N
2µÄ×Ŗ»ÆĀŹĪŖ
30%
30%
£®



 2NH3(g) ¦¤H£½£92 kJ”¤mol-1”£
2NH3(g) ¦¤H£½£92 kJ”¤mol-1”£