
题目列表(包括答案和解析)
A.ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种化合价,含ⅥA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)氧元素能形成繁多的氧化物,请写出一个与CO2等电子的化合物 ▲ 。
(2)Se原子基态核外电子的排布式为 ▲ ; O、S、Se原子的第一电离能由大到小的顺序为 ▲ ;
(3)SO32-离子中硫原子的杂化方式 ▲ ,该离子的立体构型为 ▲ ;
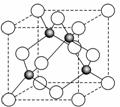
(4)某金属元素(以A表示)的氧化物用作玻璃、瓷器的颜料、脱硫剂。其立方晶体的晶胞结构如右图所示,则该氧化物的化学式为 ▲ 。
下列结论正确的是( )
①微粒半径S2->Cl>S>F ②稳定性HF>HCl>H2S>H2Fe
③还原性S2->Cl->Br->I- ④氧化性Cl2>S>Se>Fe
⑤酸性H2SO4>HClO4>H2SO3 ⑥非金属性F>Cl>S>Se
A.②④⑥ B.①③④ C.① D.⑥
|
硒被称为主宰生命的元素之一,人们开发了一种含有钙铁锌硒(Ca、Fe、Zn、Se)的保健品.下列说法正确的是 | |
| [ ] | |
A. |
四种元素均处于第四周期,且均是主族元素 |
B. |
H2Se比H2O热稳定性好 |
C. |
单质钙能从FeSO4溶液中置换出铁 |
D. |
保键品为人体提供了必需的Fe、Zn、Se等微量元素 |
硒(Se)为第四周期ⅥA族元素, 据此,Se不可能具有的性质是
[ ]
A. 在通常状况下是固体 B. SeO2的水化物是一种酸
C. 有+4、+6、-2三种常见化合价 D. H2Se比H2S稳定
①粒子半径:S2->Cl>S>F ②氢化物的稳定性,HF>HCl>H2S>H2Te ③离子的还原性:S2->Cl->Br->I- ④氧化性:Cl2>S>Se>Te ⑤酸性:H2SO4>HClO4>H2SeO4 ⑥非金属性:F>Cl>S>Se
A.②④⑥ B.①③④
C.只有① D.⑥
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com