
题目列表(包括答案和解析)
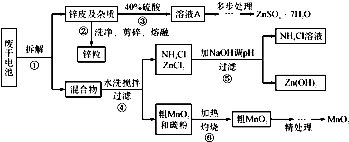
| NH3?H2O的Kb | Zn 2+完全沉淀的pH | Zn(OH)2溶于碱的pH |
| 1.8×10-5 | 8.9 | >11 |
| ||
| ||
从樟科植物枝叶提取的精油中含有下列甲、乙、丙三种成分:
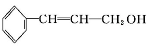
(甲)
分子式 | C9H8O |
部分性质 | 能使Br2/CCl4褪色 |
(乙)
分子式 | C16H14O2 |
部分性质 | 能使Br2/CCl4褪色 |
能在稀硫酸中水解 |
(丙)
(1)甲中所含官能团的名称为 、 。
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):
甲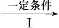
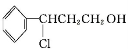
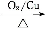 Y
Y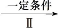 乙
乙
其中反应Ⅰ的反应类型为 ,反应Ⅰ的目的是 。
(3)已知:
RCH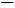 CHR'
CHR'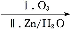 RCHO+R'CHO;2HCHO
RCHO+R'CHO;2HCHO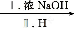 HCOOH+CH3OH
HCOOH+CH3OH
由乙制丙的一种合成路线图如下(A~F均为有机物,图中Mr表示相对分子质量):
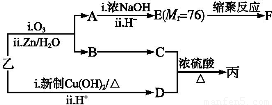
①下列物质不能与C反应的是 (选填序号)。
A.金属钠 B.HBrC.Na2CO3溶液D.乙酸
②写出由E生成F的反应方程式: ?????????????????????????????????????????????????????????? 。
③D有多种同分异构体,写出其中一种能同时满足下列条件的异构体结构简式 。
a.苯环上连接着三种不同官能团
b.能发生银镜反应
c.能与Br2/CCl4发生加成反应
d.遇FeCl3溶液显示特征颜色
④写出丙的结构简式: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com