(2010?南宁二模)氯化亚铜在氯的衍生物产品中占有较突出的位置,在有机合成工业中可作催化剂.以下是从含Cu
2+、Fe
3+的电镀废水中制备氯化亚铜的工艺流程图如图1所示.
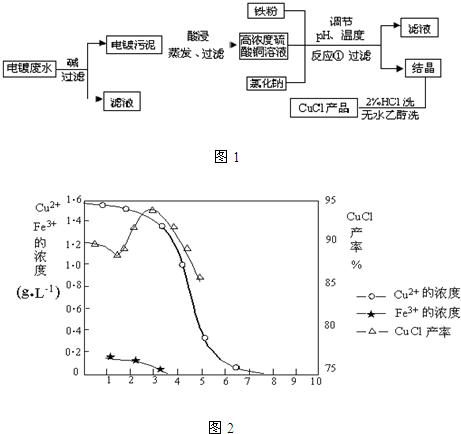
用滤液中Cu
2+、Fe
3+的含量对pH作图,可直观地反映出滤液中金属离子含量与pH之间的关系以及反应①系统pH与CuCl产率的关系(如图2).
请回答以下问题:
(1)含Cu
2+、Fe
3+的电镀废水加碱沉淀时,会有Fe(OH)
3生成.当pH=5时,在电镀废水中再加入氢氧化钠溶液生成电镀污泥的主要成分为
Cu(OH)2
Cu(OH)2
.
(2)由反应①制备CuCl时的最佳pH在
3.5
3.5
左右.
(3)对CuCl产率探究时发现反应①在隔绝空气条件下进行时CuCl产率较高,由此推测CuCl具有
还原
还原
性.
(4)反应①中1mol铁粉完全反应转移2mol电子,写出其离子反应方程式为
2Cu2++2Cl-+Fe=2CuCl↓+Fe2+
2Cu2++2Cl-+Fe=2CuCl↓+Fe2+
.如果将反应①中铁粉换为亚硫酸钠,也可以得到氯化亚铜,请完成这一反应的化学方程式
2CuSO4+Na2SO3+2NaCl+H2O=2CuCl↓+2Na2SO4+H2SO4
2CuSO4+Na2SO3+2NaCl+H2O=2CuCl↓+2Na2SO4+H2SO4
.

