
题目列表(包括答案和解析)
控制、治理氮氧化物对大气的污染是改善大气质量的重要方面。
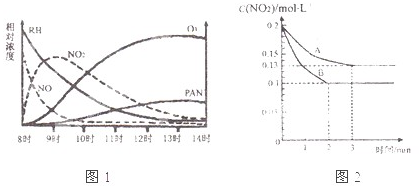
 (1)光化学烟雾白天生成,傍晚消失,其主要成分为RH(烃)、NO、NO2、O3、PAN(CH3COOONO2),某地早上至中午这些物质的相对浓度变化如右图所示,则下列叙述合理的是 。(填字母)
(1)光化学烟雾白天生成,傍晚消失,其主要成分为RH(烃)、NO、NO2、O3、PAN(CH3COOONO2),某地早上至中午这些物质的相对浓度变化如右图所示,则下列叙述合理的是 。(填字母)
a.早上8时交通繁忙期,光化学烟雾的主要成分为RH、NO
b.14时,光化学烟雾的主要成分为O3、PAN
c.PAN、O3由RH和NO直接反应生成
d.PAN直接由O3转化生成
(2)火力发电厂的燃煤排烟中含大麓的氮氧化物(NOx),可利用甲烷和NOx一定条件下反应消除其污染,则CH4与NO2反应的化学方程式为 。
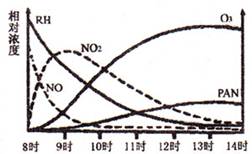
(3)在一密闭容器中发生反应2NO2![]() 2NO+O2,反应过程中NO2的浓度随时间变化的情况如右下图所示。请回答:
2NO+O2,反应过程中NO2的浓度随时间变化的情况如右下图所示。请回答:
① 依曲线A,反应在前3 min内氧气的平均反应速率为 。
② 若曲线A、B分别表示的是该反应在某不同条件下的反应情况,则此条件是 (填“浓度”、“压强”、“温度”或“催化剂”)。
③ 曲线A、B分剐对应的反应平衡常数的大小关系是![]()
![]() 。(填“>”、“<”或“=”)
。(填“>”、“<”或“=”)
(4)一定温度下,在匦容密闭容器中N2O5可发生下列反应:
2N2O5(g)![]() 4NO2(g)+O2(g) Ⅰ
4NO2(g)+O2(g) Ⅰ
2NO2(g)![]() 2NO(g)+O2(g) Ⅱ
2NO(g)+O2(g) Ⅱ
则反应Ⅰ的平衡常数表达式为 。若达平衡时,![]() (NO2)=0.4 mol?L
(NO2)=0.4 mol?L![]() ,
,![]() (O2)=1.3 mol?L
(O2)=1.3 mol?L![]() ,则反应Ⅱ中NO2的转化率为 ,N2O5(g)的起始浓度应不低于 mo1?L
,则反应Ⅱ中NO2的转化率为 ,N2O5(g)的起始浓度应不低于 mo1?L![]() 。
。
(15分)控制,治理氮氧化物对大气的污染是改善大气质量的重要方法。
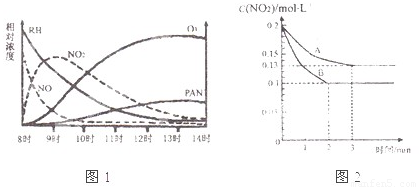
(1)某研究性学习小组在一烟雾实验箱中对光化学烟雾形成进行了模拟实验。测得烟雾的主要成分为C2H8(烃)、NO2、O3、PAN(CH3COOONO2)各种物质的相对浓度随时间的变化,记录于右图。根据图中数据,下列推论中合理的是 (填写序号)
A.NO的消耗的速率比CxHy快
B.C2H8和NO2反应可以生成PAN及O2
C.CxHy与O3反应生成PAN
(2)火力发电厂的燃煤排烟中含大量的氮氧化物(NO![]() ),可利用甲烷和NO
),可利用甲烷和NO![]() 在一定条件下反应消除其污染,则CH4与NO2反应的化学方程式为 。
在一定条件下反应消除其污染,则CH4与NO2反应的化学方程式为 。
(3)在一密闭容器中发生反应2NO22NO+O3;△H>0,反应过程中浓度随时间变化的情况如下图所示。
请回答:
①图中表示NO2的变化的曲线是 。用O2表示从O—10s内该反应的平均速率v(O2)= 。
②能说明该反应已达到平衡状态的是 。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
③第13秒钟时,改变实验条件(温度、压强、催化剂)得到温度随时间变化的曲线,则第13秒钟改变的条件是 ;
(4)一定温度下,在恒容密闭容器中N2O3可发生下列反应:
(Ⅰ)2N2O5(g)4NO2(g)+O2(g)
(Ⅱ)2NO2(g) 2NO(g)+O2(g)
若达到平衡时,c(NO2)=0.4mol·L-1,c(O2)=1.3mol·L-1,则反应Ⅱ中NO2的转化率为 。N2O5(g)的起始浓度应不低于 mol·L-1。
(15分)控制,治理氮氧化物对大气的污染是改善大气质量的重要方法。
(1)某研究性学习小组在一烟雾实验箱中对光化学烟雾形成进行了模拟实验。测得烟雾的主要成分为C2H8(烃)、NO2、O3、PAN(CH3COOONO2)各种物质的相对浓度随时间的变化,记录于右图。根据图中数据,下列推论中合理的是 (填写序号)
A.NO的消耗的速率比CxHy快
B.C2H8 和NO2反
和NO2反 应可以生成PAN及O2
应可以生成PAN及O2
C.CxHy与O3反应生成PAN
(2)火力发电厂的燃煤排烟中含大量的氮氧化物(NO ),可利用甲烷和NO
),可利用甲烷和NO 在一定条件下反应消除其污染,则CH4与NO2反应的化学
在一定条件下反应消除其污染,则CH4与NO2反应的化学 方程式为 。
方程式为 。
(3)在一密闭容器中发生反应2NO2 2NO+O3;△H>0,反应过程中浓度随时间变化的情况如下图所示。
2NO+O3;△H>0,反应过程中浓度随时间变化的情况如下图所示。
请回答:
①图中表示NO2的变化的曲线是 。用O2表示从O—10s内该反应的平均速率v(O2)= 。
②能说明该反应已达到平衡状态的是 。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
③第13秒钟时,改变实验条件(温度、压强、催化剂)得到温度随时间变化的曲线,则第13秒钟改变的条件是 ;
(4)一定温度下,在恒容密闭容器中N2O3可发生下列反应:
(Ⅰ)2N2O5(g) 4NO2(g)+O2(g)
4NO2(g)+O2(g)
(Ⅱ)2NO2(g)  2NO(g)+O2(g)
2NO(g)+O2(g)
若达到平衡时,c(NO2) =0.4mol·L-1,c(O2)=1.3mol·L-1,则反应Ⅱ中NO2的转化率为 。N2O5(g)的起始浓度应不低于 mol·L-1。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com