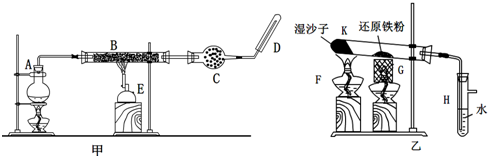
œ÷¥˙…Áª·÷–Õ≠‘⁄µÁ∆¯°¢ΩªÕ®°¢ª˙–µ∫Õ“±Ω°¢ƒÐ‘¥º∞ تØ𧓵°¢∏þø∆ººµ»¡Ï”Ú”–π„∑∫µƒ”¶”√£Æƒ≥Õ≠øÛ Ø∫¨—ıªØÕ≠°¢—ıªØ—«Õ≠°¢»˝—ıªØ∂˛Ã˙∫Õ¬ˆ Ø£®SiO
2£©£¨œ÷≤…”√À·Ω˛∑®¥”øÛ Ø÷–÷»°Õ≠£¨∆‰π§“’¡˜≥ÃÕº»Áœ¬£Æ∆‰÷–Õ≠µƒðÕ»°£®Õ≠¥”ÀÆ≤„Ω¯»Î”–ª˙≤„µƒπ˝≥ã©∫Õ∑¥ðÕ»°£®Õ≠¥””–ª˙≤„Ω¯»ÎÀÆ≤„µƒπ˝≥ã© «œ÷¥˙ ™∑®¡∂Õ≠µƒ÷ÿ“™π§“’ ÷∂Œ£Æ
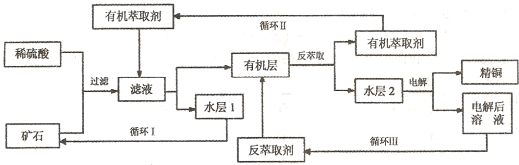
“—÷™£∫¢ŸCu
2O+2H
+=Cu
2++Cu+H
2O£ª¢⁄µ±øÛ Ø÷–»˝—ıªØ∂˛Ã˙∫¨¡øôµÕ ±£¨ø…”√¡ÚÀ·∫Õ¡ÚÀ·Ã˙µƒªÏ∫œ“∫Ω˛≥ˆÕ≠£ª¢€∑¥ðÕ»°∫ÛµƒÀÆ≤„2 «¡ÚÀ·Õ≠»Ð“∫£Æªÿ¥œ¬¡–Œ £∫
£®1£©øÛ Ø”√œ°¡ÚÀ·¥¶¿Ìπ˝≥Ã÷–∑¢…˙∑¥”¶µƒ¿Î◊”∑Ω≥Ã ΩŒ™£∫Cu
2O+2H
+=Cu
2++Cu+H
2O
CuO+2H+®TCu2++H2O
CuO+2H+®TCu2++H2O
°¢
Fe2O3+6H+®T2Fe3++3H2O£¨Cu+2Fe3++2Fe2++Cu2+£¨
Fe2O3+6H+®T2Fe3++3H2O£¨Cu+2Fe3++2Fe2++Cu2+£¨
£®2£©°∞—≠ª∑I°±æ≠∂ý¥Œ—≠ª∑∫ÛµƒÀÆ≤„1≤ªƒÐºÃ–¯—≠ª∑ π”√£¨µ´ø…∑÷¿Î≥ˆ“ª÷÷÷ÿ“™µƒ¡ÚÀ·—ŒæßãƻÙÀÆ≤„1±©¬∂‘⁄ø’∆¯÷–“ª∂Œ ±º‰∫Û£¨ø…“‘µ√µΩ¡Ì“ª÷÷÷ÿ“™µƒ¡ÚÀ·—Œ£¨–¥≥ˆÀÆ≤„l±©¬∂‘⁄ø’∆¯÷–∑¢…˙∑¥”¶µƒ¿Î◊”∑Ω≥à Ω
4Fe2++O2+4H+=4Fe3++2H2O
4Fe2++O2+4H+=4Fe3++2H2O
£Æ
£®3£©°∞—≠ª∑n°±÷–ðÕ»°º¡ «“ª¿ý≥∆◊˜Œ™Îø¿ýµƒ”–ª˙ªØ∫œŒÔ£¨»ÁN“ª510°¢N“ª530µ»£Æƒ≥Îø¿ýªØ∫œŒÔAµƒ∑÷◊”Ω·ππ÷–Ωˆ∫¨n
1∏ˆ-CH
3°¢n
2∏ˆ-OH∫Õn
3∏ˆ
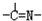
»˝÷÷ª˘Õ≈£¨ŒÞª∑◊¥Ω·π𣨻˝÷÷ª˘Õ≈µƒ ˝ƒøπÿœµŒ™n
3=
n1+n2-2
n1+n2-2
£Æ»ÙAµƒœý∂‘∑÷◊”÷ ¡øŒ™116£¨…œ ˆª˘Õ≈¡¨Ω” ±Ãº‘≠◊”∏˙ú‘≠◊”œý¡¨£¨‘ÚAµƒΩ·ππºÚ Ω «
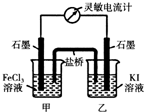
£®4£©–¥≥ˆµÁΩ‚π˝≥Ã÷–—Ùº´£®∂Ë–‘µÁº´£©∑¢…˙∑¥”¶µƒµÁº´∑¥”¶ Ω
4OH--4e-=2H2O+O2
4OH--4e-=2H2O+O2
£®5£©∏√𧓒◊Ó¥Û¡¡µ„ «À¸∑˚∫œœ¬¡–‘≠¿Ì
B
B
£Æ
A£ÆªØ—ß∆Ω∫‚ B£Æ¬Ã…´ªØ—ß C£Æ÷ ¡ø ÿ∫„ D£ÆƒÐ¡ø ÿ∫„ E£ÆœýÀ∆œý»Ð F£ÆÀ·ºÓ÷–∫Õ G£Æ—ıªØªπ‘≠∑¥”¶
£®6£©Õ≠°¢“¯°¢Ω «»À¿ý»œ ∂◊Ó‘Áµƒ»˝÷÷Ω Ù£¨“ÚŒ™∫БÁæÕ±ª»À√«”√◊˜«Æ±“£¨“Ú∂¯”–°∞ªı±“Ω Ù°±÷Æ≥∆£Æ”…”⁄Ã˙µƒΩ Ù–‘±»Õ≠°¢“¯°¢Ω«ø£¨œý∂‘∂¯—‘£¨»À¿ý»œ ∂Ã˙…‘Ọ̃ƃ≥—–æø–‘—ßœ∞–°◊ÈŒ™¡À÷§√˜Ã˙µƒΩ ÙªÓ∂Ø–‘±»Õ≠«ø£¨À˚…˺∆¡À»Áœ¬∑Ω∞∏£∫
¢ŸÃ˙∆¨÷√”⁄¡ÚÀ·Õ≠»Ð“∫÷–”–Õ≠Œˆ≥ˆ£ª
¢⁄Ã˙°¢Õ≠∫Õ¬»∆¯∑¥”¶∑÷±…˙≥…FeCl
3∫ÕCuCl
2£ª
¢€◊„¡øµƒÃ˙∑€∫ÕÕ≠∑€∫Õ≈®¡ÚÀ·∑¥”¶…˙≥…FeSO
4∫ÕCuSO
4£ª
¢ÐÕ≠∆¨÷√”⁄FeCl
3»Ð“∫÷–Õ≠∆¨÷Ω•»ÐΩ‚£ª
¢ð∞—Ã˙∆¨∫ÕÕ≠∆¨÷√”⁄ ¢”–œ°¡ÚÀ·µƒ…’±≠÷–£¨Ωª”√µºœþ¡¨Ω”£¨Ã˙∆¨…œŒÞ∆¯≈ð≤˙…˙£¨∂¯Õ≠∆¨…œ”–∆¯≈ð≤˙…˙£ª
¢Þ∞—Ã˙∆¨∫ÕÕ≠∆¨÷√”⁄ ¢”–≈®œıÀ·µƒ…’±≠÷–£¨≤¢”√µºœþ¡¨Ω”£¨Ã˙∆¨…œ”–∆¯≈ð≤˙…˙£¨∂¯Õ≠∆¨…œŒÞ∆¯≈ð≤˙…˙£Æ
“‘…œ…˺∆∫œ¿Ìµƒ”–
A
A
£Æ
A£Æ¡Ω÷÷∑Ω∞∏ B£Æ»˝÷÷∑Ω∞∏ C£ÆÀƒ÷÷∑Ω∞∏ D£ÆŒÂ÷÷∑Ω∞∏£Æ


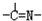 »˝÷÷ª˘Õ≈£¨ŒÞª∑◊¥Ω·π𣨻˝÷÷ª˘Õ≈µƒ ˝ƒøπÿœµŒ™n3=
»˝÷÷ª˘Õ≈£¨ŒÞª∑◊¥Ω·π𣨻˝÷÷ª˘Õ≈µƒ ˝ƒøπÿœµŒ™n3=