
题目列表(包括答案和解析)
A.加入适量NaOH固体 B.加入适量水?
C.通入适量SO2 D.加入适量CuSO4固体?
为了探究三种气态氧化物(SO2、NO2、CO2)的性质,某同学设计了一组实验:
实验一:探究三种气体在水中的溶解性,用三支相同的试管收集满三种气体,倒置在盛满水的烧杯中,一段时间后,观察到的现象如图A、B、C所示。
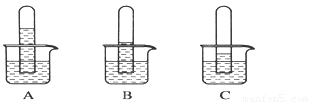
(1)在相同条件下,三种气体在水中溶解度最大的是________(写化学式)写出A烧杯中发生反应的化学方程式:____ 。如果在三只烧杯中分别滴几滴紫色石蕊试液,可观察到的现象是_____________________ 。
实验二:用三只集气瓶收集满二氧化硫、二氧化氮气体,然后将其倒置在水槽中。分别缓慢通入适量O2或Cl2,如图D、E、F所示。一段时间后,D、E装置的集气瓶中充满溶液,F装置的集气瓶中还有气体剩余。

(2)实验二中装置D的集气瓶最终充满溶液(假设瓶内液体不扩散):
①写出装置D中总反应的化学方程式:
_______________________________________________。
②假设该实验条件下,气体摩尔体积为a L·mol-1。则装置D的集气瓶中所得溶液溶质的物质的量浓度为____________________。
(3) 写出实验F通入氧气后,发生反应的化学方程式:____________________________。
(4)溶液充满集气瓶后,在E装置的水槽里滴加硝酸钡溶液,可能观察到的现象为________,用有关的离子方程式解释原因:________________________。
20℃时,H2S的饱和溶液1L,浓度约0.1 mol·L-1,其电离方程式第一步为:H2S![]() H++HS-;第二步:HS-
H++HS-;第二步:HS-![]() H++S2-,若使溶液H+、S2-浓度同时减小,可采取的措施是( )
H++S2-,若使溶液H+、S2-浓度同时减小,可采取的措施是( )
A.加入适量NaOH固体 B.加入适量水
C.通入适量SO2 D.加入适量CuSO4固体
A.加入适量NaOH固体 B.加入适量水
C.通入适量SO2 D.加入适量CuSO4固体
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com