
题目列表(包括答案和解析)
已知结构为正四面体型的离子E和直线型离子G反应,生成三角锥分子L和V形分子M(组成E、G、L、M微粒的元素原子序数均小于10),反应过程用下图表示,则下列判断错误的是 ( )

A.E、G、L、M都是10e![]() 微粒 B.L、M都是极性分子
微粒 B.L、M都是极性分子
C.L能使紫色石蕊试液变蓝色 D.E离子中,质子数一定大于中子数
| 元素代号 | A | B | C | D | E | G | L | I |
| 原子半径/nm | 0.111 | 0.064 | 0.117 | 0.16 | 0.066 | 0.070 | 0.104 | 0.077 |
| 主要化合价 | +2 | -1 | +4,-4 | +2 | -2 | +5.-3 | +6,-2 | +4,-4 |
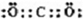
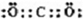
| 2 | 3 |
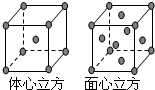 I:氮元素可以形成多种化合物.回答以下问题:
I:氮元素可以形成多种化合物.回答以下问题:湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com