
题目列表(包括答案和解析)
 氧气
氧气 氧化物甲”的转化,反应I的化学方程式为 。
氧化物甲”的转化,反应I的化学方程式为 。
| A.澄清石灰水变浑浊 | B.反应前后D中质量减轻 |
| C.F导管口有蓝色火焰 | D.加热时,四氧化三铁变红 |
(8分)在研究氧气的性质时,同学们发现含氧元素的质量可以相互转化,如“氧化物甲 氧气
氧气 氧化物甲”的转化,反应I的化学方程式为 。
氧化物甲”的转化,反应I的化学方程式为 。
【提出问题】铁丝能在氧气中燃烧,观察到火星四射、剧烈燃烧 。能不能将燃烧产物四氧化三铁再转化为铁单质呢?
【查阅资料】(1)Fe3O4的分解温度为1538 oC
(2)CO具有还原性,能将某些金属氧化物还原为金属单质
(3)酒精灯外焰温度约700 oC,酒精喷灯火焰温度约1000 oC
(4)铁丝为银白色,铁粉为黑色
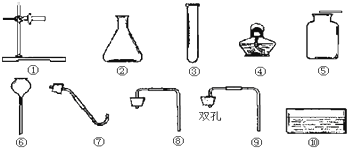
【设计实验】同学们设计了如下图所示的实验装置,对CO能不能将四氧化三铁转化为铁进行探究。结合图示回答问题。
(1)B装置中浓硫酸具有吸水性,能除去二氧化碳中的水蒸气,浓硫酸吸水过程会 (填“吸热”或“放热”)。
(2)C装置可将二氧化碳转化为一氧化碳,反应的化学方程式为 。
(3)F处点燃酒精的目的是 。
(4)依据现象得出结论,该设计中观察到以下现象,其中可以说明四氧化三铁与一氧化碳发生反应的现象是 (填字母序号)。
| A.澄清石灰水变浑浊 | B.反应前后D中质量减轻 |
| C.F导管口有蓝色火焰 | D.加热时,四氧化三铁变红 |
(8分)在研究氧气的性质时,同学们发现含氧元素的质量可以相互转化,如“氧化物甲 氧气
氧气 氧化物甲”的转化,反应I的化学方程式为 。
氧化物甲”的转化,反应I的化学方程式为 。
【提出问题】铁丝能在氧气中燃烧,观察到火星四射、剧烈燃烧 。能不能将燃烧产物四氧化三铁再转化为铁单质呢?
【查阅资料】(1)Fe3O4的分解温度为1538 oC
(2)CO具有还原性,能将某些金属氧化物还原为金属单质
(3)酒精灯外焰温度约700 oC,酒精喷灯火焰温度约1000 oC
(4)铁丝为银白色,铁粉为黑色
【设计实验】同学们设计了如下图所示的实验装置,对CO能不能将四氧化三铁转化为铁进行探究。结合图示回答问题。
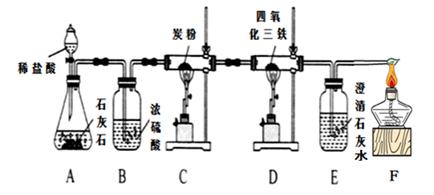
(1)B装置中浓硫酸具有吸水性,能除去二氧化碳中的水蒸气,浓硫酸吸水过程会 (填“吸热”或“放热”)。
(2)C装置可将二氧化碳转化为一氧化碳,反应的化学方程式为 。
(3)F处点燃酒精的目的是 。
(4)依据现象得出结论,该设计中观察到以下现象,其中可以说明四氧化三铁与一氧化碳发生反应的现象是 (填字母序号)。
A.澄清石灰水变浑浊 B.反应前后D中质量减轻
C.F导管口有蓝色火焰 D.加热时,四氧化三铁变红
【反思与评价】由于上述实验设计有明显不足,致使某些现象不能作为推理的依据,其中的不足是 。
| ||
| ||
| ||
纯碱(![]() )产品中常含有少量氯化钠。某厂生产的纯碱包装袋上标有“
)产品中常含有少量氯化钠。某厂生产的纯碱包装袋上标有“![]() 含量≥95%”字样。为判断该产品中
含量≥95%”字样。为判断该产品中![]() 的含量是否达到要求,称取5.0g样品进行检验,可供选取的装置如下图。其中,丙装置中装足量浓氢氧化钠溶液,丁装置中装浓硫酸,戊装置中装水。(提示:浓硫酸具有吸水性,不挥发,不与二氧化碳反应,碳酸钠受热不分解。)
的含量是否达到要求,称取5.0g样品进行检验,可供选取的装置如下图。其中,丙装置中装足量浓氢氧化钠溶液,丁装置中装浓硫酸,戊装置中装水。(提示:浓硫酸具有吸水性,不挥发,不与二氧化碳反应,碳酸钠受热不分解。)
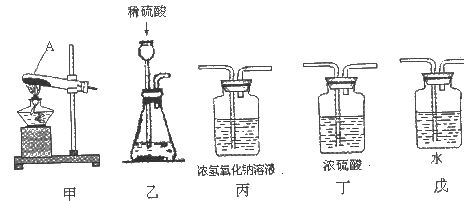
(1)写出上图仪器A的一种常见用途___________。
(2)你选择的实验装置从左到右组装排列为(填编号)___________。请说出你选择或排列装置的一点理由_________。
(3)假设每步都反应完全,生成的二氧化碳全部被吸收,不考虑空气中二氧化碳的影响。较准确地计算“![]() 含量≥95%”是否真实,该实验除称取样品质量外,还要用天平量得到的实验数据是 _________。
含量≥95%”是否真实,该实验除称取样品质量外,还要用天平量得到的实验数据是 _________。
(4)若乙装置中加入浓盐酸(有挥发性),对测量结果会产生影响。原因是浓盐酸挥发出的氯化氢气体__________。
(5)若实验装置连接正确,实验过程中看到丙装置出现的气泡比丁少得多,一种可能的原_____________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com