
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
 AΓΔBΓΔCΓΔDΓΔEΈε÷÷ΕΧ÷ήΤΎ‘ΣΥΊΘ§‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΘ§AΓΔEΆ§÷ςΉεΘ§A‘ΣΥΊΒΡ‘≠Ή”ΑκΨΕΉν–ΓΘ§B‘ΣΥΊ‘≠Ή”ΒΡΉνΆβ≤ψΒγΉ” ΐ «ΡΎ≤ψΒγΉ” ΐΒΡ2±ΕΘ§C‘ΣΥΊΒΡΉνΗΏΦέ―θΜ·ΈοΒΡΥ°Μ·ΈοX”κΤδ«βΜ·ΈοΖ¥”Π…ζ≥…“Μ÷÷―ΈYΘ§AΓΔBΓΔCΓΔEΥΡ÷÷‘ΣΥΊΕΦΡή”κD‘ΣΥΊ–Έ≥…‘≠Ή”Ηω ΐ±»≤ΜœύΆ§ΒΡ≥ΘΦϊΜ·ΚœΈοΘ°ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
AΓΔBΓΔCΓΔDΓΔEΈε÷÷ΕΧ÷ήΤΎ‘ΣΥΊΘ§‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΘ§AΓΔEΆ§÷ςΉεΘ§A‘ΣΥΊΒΡ‘≠Ή”ΑκΨΕΉν–ΓΘ§B‘ΣΥΊ‘≠Ή”ΒΡΉνΆβ≤ψΒγΉ” ΐ «ΡΎ≤ψΒγΉ” ΐΒΡ2±ΕΘ§C‘ΣΥΊΒΡΉνΗΏΦέ―θΜ·ΈοΒΡΥ°Μ·ΈοX”κΤδ«βΜ·ΈοΖ¥”Π…ζ≥…“Μ÷÷―ΈYΘ§AΓΔBΓΔCΓΔEΥΡ÷÷‘ΣΥΊΕΦΡή”κD‘ΣΥΊ–Έ≥…‘≠Ή”Ηω ΐ±»≤ΜœύΆ§ΒΡ≥ΘΦϊΜ·ΚœΈοΘ°ΜΊ¥πœ¬Ν–Έ ΧβΘΚ“―÷ΣAΓΔBΓΔCΓΔDΓΔEΓΔFΝυ÷÷ΕΧ÷ήΤΎ‘ΣΥΊΒΡ–‘÷ ΜρΫαΙΙ–≈œΔ»γœ¬±μΘ§«κΗυΨί–≈œΔΜΊ¥πœ¬Ν–Έ ΧβΓΘ
‘ΣΥΊ –‘÷ ΜρΫαΙΙ–≈œΔ
A ΒΞ÷ ≥ΘΈ¬œ¬ΈΣΙΧΧεΘ§Ρ―»ή”ΎΥ°“Ή”Ύ»ήCS2ΓΘΡή–Έ≥…2÷÷Εΰ‘ΣΚ§―θΥαΓΘ
B ‘≠Ή”ΒΡM≤ψ”–1ΗωΈ¥≥…Ε‘ΒΡpΒγΉ”ΓΘΚΥΆβpΒγΉ”Ήή ΐ¥σ”Ύ7ΓΘ
C ΒΞ÷ ‘χ±Μ≥ΤΈΣΓΑ“χ…ΪΒΡΫπΉ”Γ±ΓΘ”κο°–Έ≥…ΒΡΚœΫπ≥Θ”Ο”ΎΚΫΧλΖ…––ΤςΓΘΒΞ÷ Ρή»ή«ΩΥαΚΆ«ΩΦνΓΘ
D ‘≠Ή”ΚΥΆβΒγΉ”≤ψ…œsΒγΉ”Ήή ΐ±»pΒγΉ”Ήή ΐ…Ό2ΗωΓΘΒΞ÷ ΚΆ―θΜ·ΈοΨυΈΣΩ’ΦδΆχΉ¥ΨßΧεΘ§ΨΏ”–ΚήΗΏΒΡ»έΓΔΖ–ΒψΓΘ
E Τδ―θΜ·Έο «Τϊ≥ΒΈ≤ΤχΒΡ÷ς“Σ”–ΚΠ≥…Ζ÷÷°“ΜΘ§“≤ «Ω’Τχ÷ ΝΩ‘Λ±®ΒΡ÷Η±ξ÷°“ΜΘΜΗΟ‘ΣΥΊ‘Ύ»ΐΨέ«ηΑΖ÷–Κ§ΝΩΫœΗΏΓΘ
F ÷ήΤΎ±μ÷–ΒγΗΚ–‘Ήν¥σΒΡ‘ΣΥΊ
Θ®1Θ©A‘≠Ή”ΒΡΉνΆβ≤ψΒγΉ”≈≈≤Φ Ϋ Θ§D‘≠Ή”Ι≤”– ÷÷≤ΜΆ§‘ΥΕ·Ή¥Χ§ΒΡΒγΉ”ΓΘ
Θ®2Θ©F”κE‘ΣΥΊΒΎ“ΜΒγάκΡήΒΡ¥σ–ΓΙΊœΒΘΚ ΘΨ Θ®Χν‘ΣΥΊΖϊΚ≈Θ©ΓΘ
Θ®3Θ©AΘ§BΝΫ‘ΣΥΊΒΡ«βΜ·ΈοΖ÷Ή”÷–ΦϋΡήΫœ–ΓΒΡ « ΘΜΖ÷Ή”ΫœΈ»Ε®ΒΡ « ΓΘΘ®ΧνΖ÷Ή” ΫΘ©
Θ®4Θ©CΒΞ÷ ΓΔΟΨΓΔNaOH»ή“ΚΩ…“‘ΙΙ≥…‘≠Βγ≥ΊΘ§‘ρΗΚΦΪΒΡΒγΦΪΖ¥”Π ΫΈΣ_________________ΓΘ
Θ®5Θ©F”κΗΤΩ…Ήι≥…άκΉ”Μ·ΚœΈοΘ§ΤδΨßΑϊΫαΙΙ»γΆΦΥυ ΨΘ§ΗΟΜ·ΚœΈοΒΡΒγΉ” Ϋ « ΓΘ“―÷ΣΗΟΜ·ΚœΈοΨßΑϊ1/8ΒΡΧεΜΐΈΣ2.0ΓΝ10-23cm3Θ§«σΗΟάκΉ”Μ·ΚœΈοΒΡΟήΕ»Θ§«κΝ– Ϋ≤ΔΦΤΥψΘ®ΫαΙϊ±ΘΝτ“ΜΈΜ–Γ ΐΘ©ΘΚ_______________________ΓΘ

| ‘ΣΥΊ | –‘÷ ΜρΫαΙΙ–≈œΔ |
| A | ΒΞ÷ ≥ΘΈ¬œ¬ΈΣΙΧΧεΘ§Ρ―»ή”ΎΥ°“Ή”Ύ»ήCS2ΓΘΡή–Έ≥…2÷÷Εΰ‘ΣΚ§―θΥαΓΘ |
| B | ‘≠Ή”ΒΡM≤ψ”–1ΗωΈ¥≥…Ε‘ΒΡpΒγΉ”ΓΘΚΥΆβpΒγΉ”Ήή ΐ¥σ”Ύ7ΓΘ |
| C | ΒΞ÷ ‘χ±Μ≥ΤΈΣΓΑ“χ…ΪΒΡΫπΉ”Γ±ΓΘ”κο°–Έ≥…ΒΡΚœΫπ≥Θ”Ο”ΎΚΫΧλΖ…––ΤςΓΘΒΞ÷ Ρή»ή«ΩΥαΚΆ«ΩΦνΓΘ |
| D | ‘≠Ή”ΚΥΆβΒγΉ”≤ψ…œsΒγΉ”Ήή ΐ±»pΒγΉ”Ήή ΐ…Ό2ΗωΓΘΒΞ÷ ΚΆ―θΜ·ΈοΨυΈΣΩ’ΦδΆχΉ¥ΨßΧεΘ§ΨΏ”–ΚήΗΏΒΡ»έΓΔΖ–ΒψΓΘ |
| E | Τδ―θΜ·Έο «Τϊ≥ΒΈ≤ΤχΒΡ÷ς“Σ”–ΚΠ≥…Ζ÷÷°“ΜΘ§“≤ «Ω’Τχ÷ ΝΩ‘Λ±®ΒΡ÷Η±ξ÷°“ΜΘΜΗΟ‘ΣΥΊ‘Ύ»ΐΨέ«ηΑΖ÷–Κ§ΝΩΫœΗΏΓΘ |
| F | ÷ήΤΎ±μ÷–ΒγΗΚ–‘Ήν¥σΒΡ‘ΣΥΊ |


2012ΡξΕ§ΦΨΘ§Έ“Ιζ≥« –Ω’ΤχΈέ»ΨΉ¥Ωω ήΒΫ»ΥΟ«ΒΡ«ΩΝ“ΙΊΉΔΘ§Τδ÷–NOxΓΔCOΓΔSO2 «÷ς“ΣΈέ»Ψ–‘ΤχΧεΓΘ
IΘ°Τϊ≥ΒΡΎ»ΦΜζΙΛΉς ±ΖΔ…ζΒΡΖ¥”Π «ΒΦ÷¬Τϊ≥ΒΈ≤ Τχ÷–Κ§”–NOΒΡ÷Ί“Σ‘≠“ρ÷°“ΜΓΘ
«ΒΦ÷¬Τϊ≥ΒΈ≤ Τχ÷–Κ§”–NOΒΡ÷Ί“Σ‘≠“ρ÷°“ΜΓΘ
Θ®1Θ©”–»Υ”ϊ―Γ”ΟΚœ ΒΡ¥ΏΜ·ΦΝΘ§ ΙΖ¥”Π2NOΘ®gΘ©=N2Θ®gΘ©+O2Θ®gΘ©ΡήΫœΩλΫχ––“‘¥οΒΫ≥ΐ»ΞNOΒΡΡΩΒΡΓΘΡψ»œΈΣΗΟΖ¥”ΠΡήΖώΉ‘ΖΔΫχ–– Θ®ΧνΓΑΡήΓ±ΜρΓΑ≤ΜΡήΓ±Θ©ΓΘ
Θ®2Θ©άϊ”Ο¥ΏΜ·ΦΦ θΩ…ΫΪΤϊ≥ΒΈ≤Τχ÷–ΒΡNOΤχΧεΉΣΜ·≥…ΈόΕΨΤχΧεΘ§œύΙΊΖ¥”ΠΒΡΤΫΚβ≥Θ ΐΩ…±μ ΨΈΣ
 Θ§¥ΥΖ¥”ΠΈΣΖ≈»»Ζ¥”ΠΓΘ‘Ύ“ΜΕ®Έ¬Ε»œ¬Θ§10LΡ≥Οή±’»ίΤς÷–ΖΔ…ζ…œ ωΖ¥”ΠΘ§ΗςΈο÷ ΒΡΈο÷ ΒΡΝΩΒΡ±δΜ·«ιΩω»γœ¬±μ
Θ§¥ΥΖ¥”ΠΈΣΖ≈»»Ζ¥”ΠΓΘ‘Ύ“ΜΕ®Έ¬Ε»œ¬Θ§10LΡ≥Οή±’»ίΤς÷–ΖΔ…ζ…œ ωΖ¥”ΠΘ§ΗςΈο÷ ΒΡΈο÷ ΒΡΝΩΒΡ±δΜ·«ιΩω»γœ¬±μ

ΔΌΗυΨίΆΝ±μ ΐΨίΦΤΥψ0~4sΦδ”ΟNO±μ ΨΒΡΤΫΨυΥΌ¬ vΘ®NOΘ©= ΘΜ¥οΒΫΜ·―ßΤΫΚβ ±ΝΫ÷÷Ζ¥”ΠΈοΒΡΉΣΜ·¬ «ΖώœύΒ» Θ®ΧνΓΑœύȖΜρΓΑ≤Μœύ»ñȩΓΘ
ΔΎ‘Ύ5~6s ±Θ§»τK‘ω¥σΘ§5sΚσ’ΐΖ¥”ΠΥΌ¬ Θ®ΧνΓΑ‘ω¥σΓ±ΜρΓΑΦθ–ΓΓ±Θ©
Δέ‘Ύ5~6s ±Θ§»τK≤Μ±δΘ§“‘…œΗςΈο÷ ΒΡΈο÷ ΒΡΝΩ±δΜ·‘≠“ρΩ…Ρή « ΓΘ
AΘ°―Γ”ΟΗϋ”––ßΒΡ¥ΏΜ·ΦΝ BΘ°Υθ–Γ»ίΤςΒΡΧεΜΐ
CΘ°ΫΒΒΆCO2≈®Ε» DΘ°…ΐΗΏΈ¬Ε»
IIΈΣΧΫΨΩΝρ‘Ύ―θΤχ÷–»Φ…’ΒΡ≤ζΈοάο «Ζώ”–SO3Θ§Ρ≥Μ·―ß–Υ»Λ–ΓΉι‘ΎΨχ»»ΜΖΨ≥œ¬Ϋχ––ΝΥΕ®ΝΩ Β―ιΧΫΨΩΓΘΧΫΨΩ Β―ιΒΡœύΙΊ ΐΨί»γœ¬
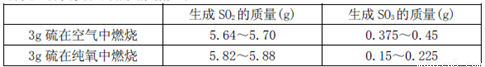
Θ®3Θ©Ε‘ ΐΨίΫχ––Ζ÷ΈωΩ…÷ΣΘ§Β»÷ ΝΩΒΡΝρ‘Ύ¥Ω―θ÷–»Φ…’≤ζ…ζΒΡSO3±»‘ΎΩ’Τχ÷–»Φ…’≤ζ…ζΒΡSO3 Θ®ΧνΓΑΕύΓ±ΜρΓΑ…ΌΓ±Θ©Θ§‘≠“ρΩ…Ρή « ΓΘ
AΘ°¥Ω―θ÷–―θΤχ≈®Ε»ΗΏΘ§”–άϊ”ΎΜ·―ßΤΫΚβ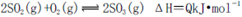 œρ”““ΤΕ·
œρ”““ΤΕ·
BΘ°Μ·―ßΖ¥”Π
CΘ°¥Ω―θ÷–―θΤχ≈®Ε»ΗΏΘ§ΒΞΈΜ ±ΦδΡΎΖΔ»»ΝΩ¥σΘ§÷¬ ΙΖ¥”ΠΧεœΒΒΡΈ¬Ε»ΫœΗΏΘ§≤Μάϊ”ΎΜ·―ßΤΫΚβ
 œρ”““ΤΕ·
œρ”““ΤΕ·
DΘ°3gΝρ‘Ύ¥Ω―θ÷–»Φ…’±»3gΝρ‘ΎΩ’Τχ÷–»Φ…’Ζ≈≥ωΒΡ»»ΝΩΕύΘ§≤Μάϊ”ΎΜ·―ßΤΫΚβ
 œρ”““ΤΕ·
œρ”““ΤΕ·
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com