
ÌâÄ¿Áбí(°üÀ¨´ð°¸ºÍ½âÎö)
ÒÑÖª2NO2![]() N2O4£«Q£®½«NO2³äÈëÈÝÒ×µ¼ÈȵIJÄÁÏÖƳɵÄÈÝÆ÷aºÍbÖнøÐз´Ó¦£®aµÄÈÝ»ý±£³Ö²»±ä£¬bµÄÉϸǿÉËæÈÝÆ÷ÄÚÆøÌåѹǿµÄ¸Ä±ä¶øÉÏÏÂÒƶ¯£¬ÒÔ±£³ÖÈÝÆ÷ÄÚÍâѹǿÏàµÈ£®
N2O4£«Q£®½«NO2³äÈëÈÝÒ×µ¼ÈȵIJÄÁÏÖƳɵÄÈÝÆ÷aºÍbÖнøÐз´Ó¦£®aµÄÈÝ»ý±£³Ö²»±ä£¬bµÄÉϸǿÉËæÈÝÆ÷ÄÚÆøÌåѹǿµÄ¸Ä±ä¶øÉÏÏÂÒƶ¯£¬ÒÔ±£³ÖÈÝÆ÷ÄÚÍâѹǿÏàµÈ£®
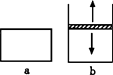
µ±Í¬ÎÂͬѹʱ£¬½«µÈÁ¿µÄNO2³äÈë¡°Æðʼ̬¡±Ìå»ýÏàͬµÄÈÝÆ÷a¡¢bÖУ¬·´Ó¦Í¬Ê±¿ªÊ¼£®
(1)·´Ó¦¿ªÊ¼Ê±£¬aÓëbÖÐÉú³ÉN2O4µÄËÙÂÊva________vb£®
(2)·´Ó¦¹ý³ÌÖÐÁ½ÈÝÆ÷ÀïÉú³ÉN2O4µÄËÙÂÊÊÇva________vb£®
(3)´ïµ½Æ½ºâʱ£¬aÓëbÖÐNO2ת»¯ÎªN2O4µÄ°Ù·ÖÊý(A)Ïà±È½Ï£¬ÔòÊÇAa________Ab£®
. |
| v |
 [»¯Ñ§-Ñ¡ÐÞÎïÖʽṹÓëÐÔÖÊ]
[»¯Ñ§-Ñ¡ÐÞÎïÖʽṹÓëÐÔÖÊ] [»¯Ñ§Ñ¡ÐÞ3£ºÎïÖʽṹÓëÐÔÖÊ]
[»¯Ñ§Ñ¡ÐÞ3£ºÎïÖʽṹÓëÐÔÖÊ]¹ú¼ÊѧУÓÅÑ¡ - Á·Ï°²áÁбí - ÊÔÌâÁбí
ºþ±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨Æ½Ì¨ | ÍøÉÏÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | µçÐÅթƾٱ¨×¨Çø | ÉæÀúÊ·ÐéÎÞÖ÷ÒåÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com