
题目列表(包括答案和解析)
CuO+2HCl====CuCl2+H2O,FeO+2HCl====FeCl2+H2O。
已知:一般地,pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥4.4时,Cu2+开始以Cu(OH)2的形式沉淀;pH≥6.4时,Cu2+以Cu(OH)2形式完全沉淀;pH在3—4时,Fe3+以Fe(OH)3的形式完全沉淀。
(1)为除去溶液中Fe2+,可采用的方法是______________________________;
(2)工业上为除去溶液中的Fe2+,常使用NaClO,当向溶液中加入NaClO后,溶液的pH变化是___________;
(3)若此溶液中杂质只有Fe3+时,要调整pH在3—4之间,此时最好向溶液中加入___________。
(4)已知溶液中c(Cu2+)与溶液pH的关系为lgc(Cu2+)=8.6-2pH,若某溶液中c(Cu2+)为1 mol·L-1,要保证此溶液中Cu2+刚好不发生沉淀,则溶液的pH应为___________,此时溶液中的铁离子能否沉淀完全___________(填“能”或“否”)。
| ||
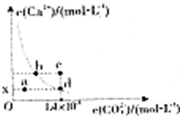 25℃时,CaCO3在水中的溶解平衡曲线如图所示.已知25℃时,CaCO3的Ksp=2.8×10-9.据图分析,下列说法不正确的是( )
25℃时,CaCO3在水中的溶解平衡曲线如图所示.已知25℃时,CaCO3的Ksp=2.8×10-9.据图分析,下列说法不正确的是( )| A、x的数值为2×10-5 | B、c点时有碳酸钙沉淀生成 | C、b点与d点对应的溶度积相等 | D、加入蒸馏水可使溶液由d点变到a点 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com