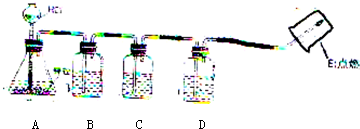现有以下与气体相关的装置、仪器和药品.请根据要求回答问题:

(1)图A的实验室制氧气装置有两处错误,请任选一处进行改正:
试管口应略向下倾斜(或试管口应塞一团棉花)
试管口应略向下倾斜(或试管口应塞一团棉花)
.
(2)装置B中反应的化学方程式为
CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
;把H与B组合,操作弹簧夹可以使反应停止或发生,还可以从“C至H”中选择仪器
CEH
CEH
(填序号)组装一个可随时使反应发生或停止的装置;若用H
2O
2和MnO
2制取O
2,且能获得平稳的气流,应选E(或F)和
D
D
组合.
(3)若用图I所示医用塑料袋排空气法收集H
2,
则H
2导入端为
b
b
(填“a”或“b”).
(4)用图J所示矿泉水瓶可以证明CO
2与NaOH溶液确实发生了反应,其现象是
矿泉水瓶变瘪
矿泉水瓶变瘪
,应做的对比实验是
取与J同样的装置,把其中的NaOH溶液换成蒸馏水.
取与J同样的装置,把其中的NaOH溶液换成蒸馏水.
.
(5)H
2和CO的混合气体共2g与30g O
2混合后,在密闭容器中完全燃烧,再冷却至室温,测得容器中混合气体的质量为23g,反应中氧气有剩余,求:反应后混合气体中各气体的质量(保留一位小数).

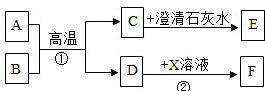
 右图是关于铁化学性质的知识网络(“→”表示一种物质转化为另一种物质),其中B是密度最小的气体,C为紫红色固体单质.请回答下列问题:
右图是关于铁化学性质的知识网络(“→”表示一种物质转化为另一种物质),其中B是密度最小的气体,C为紫红色固体单质.请回答下列问题: