
题目列表(包括答案和解析)
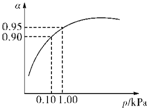 硫酸生产主要有硫磺法和硫铁矿法等,这两种制法均经过催化氧化步骤.
硫酸生产主要有硫磺法和硫铁矿法等,这两种制法均经过催化氧化步骤.| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2molSO2、1molO2 | 2molSO3 | mmolSO2、nmolO2、pmolSO3 |
| c(SO3)/mol?L-1 | 1.4 | 1.4 | 1.4 |
| 能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| SO2或SO3的转化率 | α1 | α2 | 12.5% |
| A、用分液漏斗分离乙醇和苯酚的混合物 | B、实验室用加热饱和FeCl3溶液制Fe(OH)3胶体 | C、中和滴定时滴定管用所盛溶液润洗,锥形瓶不用所盛溶液润洗 | D、用37%(p=1.19 g?cm-3)的浓盐酸配制100 mL 1 mol?L-1的盐酸溶液,用到的量器为100 mL的量筒和100 mL的容量瓶 |
| ① | He-268.8 | Ne-249.5 | Ar(x) | Kr-151.7 |
| ② | F2-187.0 | Cl2-33.6 | (a)58.7 | I2-184.0 |
| ③ | HF(Y) | HCl-84.0 | HBr-67.0 | HI-35.3 |
| ④ | H2O(Z) | H2S-60.2 | (b)-42.0 | H2Te-1.8 |

| 温度(°C) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.197 |
下列做法正确的是 ( )
A.用分液漏斗分离乙醇和苯酚的混合物
B.实验室用加热饱和FeCl3溶液制Fe(OH)3胶体
C.中和滴定时滴定管用所盛溶液润洗,锥形瓶不用所盛溶液润洗
D.用37%(p=1.19 g·cm-3)的浓盐酸配制100 mL l mol·L-1的盐酸溶液,用到的量器为100 mL的量筒和100 mL的容量瓶
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com