
题目列表(包括答案和解析)
| (2013?天津)为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚.反应原理如下: 电池:Pb(s)+PbO2(s)+2H2SO4(aq)═2PbSO4(s)+2H2O (l) 电解池:2Al+3H2O
电解过程中,以下判断正确的是( )
|
| 选项 | 方程式 | 结论 |
| A | 4Fe(OH)2+O2+2H2O=4Fe(OH)3 | Fe(OH)2不稳定易被氧化 |
| B | Al3++3NH3?H2O(过量)=Al(OH)3↓+3NH4+ | Al(OH)3不溶于碱 |
| C | 3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O | HNO3具有强氧化性 |
| D | Al2O3+6H+=2Al3++3H2O Al2O3+2OH-=2AlO2-+H2O |
Al2O3是两性氧化物 |
| A、A | B、B | C、C | D、D |
| ||
| 电池 | 电解池 | |
| A | H+移向Pb电极 | H+移向Pb电极 |
| B | 每消耗3mol Pb | 生成2mol Al2O3 |
| C | 正极:PbO2+4H++2e-═Pb2++2H2O | 阳极:2Al+3H2O-6e-═Al2O3+6H+ |
| D | 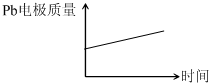 |
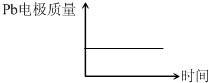 |
| A.A | B.B | C.C | D.D |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com