
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
ФГбЧСђЫсФЦЪдМСЃЌвбВПЗжБЛбѕЛЏЃЌЮЊШЗЖЈЦфДПЖШЃЌвЊНјааШчЯТЪЕбщЃКЂйГЦШЁбљЦЗ![]() ЁЁЂкНЋбљЦЗШмНтЁЁЂлШмвКжаМгШыЩдЙ§СПЕФОбЮЫсЫсЛЏЕФ
ЁЁЂкНЋбљЦЗШмНтЁЁЂлШмвКжаМгШыЩдЙ§СПЕФОбЮЫсЫсЛЏЕФ![]() ШмвКЁЁЂмЙ§ТЫЁЂЯДЕгЁЂИЩдяЁЂГСЕэЃЌГЦЦфжЪСПЮЊ
ШмвКЁЁЂмЙ§ТЫЁЂЯДЕгЁЂИЩдяЁЂГСЕэЃЌГЦЦфжЪСПЮЊ![]() ЃЌдђЃК
ЃЌдђЃК
(1)![]() вЊгУбЮЫсЫсЛЏЕФдвђЪЧ________ЃЛ
вЊгУбЮЫсЫсЛЏЕФдвђЪЧ________ЃЛ
(2)![]() ШмвКвЊЩдЙ§СПЕФдвђЪЧ________ЃЛ
ШмвКвЊЩдЙ§СПЕФдвђЪЧ________ЃЛ
(3)ХаЖЯВйзїЂлЪЧЗёЭъГЩЕФЗНЗЈЪЧ________ЃЛ
(4)ХаЖЯГСЕэЪЧЗёЯДОЛЕФЗНЗЈЪЧ________ЃЛ
(5)![]() ДПЖШЕФБэДяЪН
ДПЖШЕФБэДяЪН![]() =________ЁЃ
=________ЁЃ
ЂйГЦШЁбљЦЗW1gЃЛ
ЂкНЋбљЦЗШмНтЃЛ
ЂлИјШмвКМгШыЩдЙ§СПбЮЫсЫсЛЏСЫЕФBaCl2ШмвКЃЛ
ЂмЙ§ТЫЁЂЯДЕгЁЂИЩдяГСЕэЃЌГЦЦфжЪСПЮЊW2gЁЃЪдЛиД№ЃК
ЃЈ1ЃЉBaCl2вЊгУбЮЫсЫсЛЏЕФдвђЪЧ________ЁЃ
ЃЈ2ЃЉBaCl2ШмвКвЊЩдЙ§СПЕФдвђЪЧ________ЁЃ
ЃЈ3ЃЉХаЖЯВйзїЂлЪЧЗёЭъГЩЕФЗНЗЈЪЧ________ЁЃ
ЃЈ4ЃЉХаЖЯГСЕэЪЧЗёЯДОЛЕФЗНЗЈЪЧ________ЁЃ
ЃЈ5ЃЉNa2SO3ДПЖШБэЪОЪНЮЊ________________ЁЃ
ФГбЧСђЫсФЦЪдМСвбВПЗжБЛбѕЛЏЁЃЮЊШЗЖЈЫќЕФДПЖШЃЌвЊНјааШчЯТЪЕбщЃК
ЂйГЦШЁбљЦЗW1gЃЛ
ЂкНЋбљЦЗШмНтЃЛ
ЂлИјШмвКМгШыЩдЙ§СПбЮЫсЫсЛЏСЫЕФBaCl2ШмвКЃЛ
ЂмЙ§ТЫЁЂЯДЕгЁЂИЩдяГСЕэЃЌГЦЦфжЪСПЮЊW2gЁЃЪдЛиД№ЃК
ЃЈ1ЃЉBaCl2вЊгУбЮЫсЫсЛЏЕФдвђЪЧ________ЁЃ
ЃЈ2ЃЉBaCl2ШмвКвЊЩдЙ§СПЕФдвђЪЧ________ЁЃ
ЃЈ3ЃЉХаЖЯВйзїЂлЪЧЗёЭъГЩЕФЗНЗЈЪЧ________ЁЃ
ЃЈ4ЃЉХаЖЯГСЕэЪЧЗёЯДОЛЕФЗНЗЈЪЧ________ЁЃ
ЃЈ5ЃЉNa2SO3ДПЖШБэЪОЪНЮЊ________________ЁЃ
(15Зж)НЙбЧСђЫсФЦ(Na2S2O5)ЪЧГЃгУЕФЪГЦЗПЙбѕЛЏМСжЎвЛЁЃФГбаОПаЁзщНјааШчЯТЪЕбщЃК
ЪЕбщвЛ НЙбЧСђЫсФЦЕФжЦШЁ
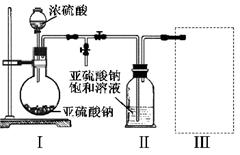
ВЩгУгвЭМзАжУ(ЪЕбщЧАвбГ§ОЁзАжУФкЕФПеЦј)жЦШЁNa2S2O5ЁЃзАжУЂђжагаNa2S2O5ОЇЬхЮіГіЃЌЗЂЩњЕФЗДгІЮЊЃКNa2SO3ЃЋSO2ЃНNa2S2O5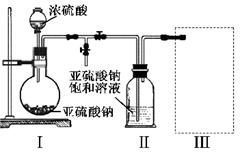
ЃЈ1ЃЉзАжУIжаВњЩњЦјЬхЕФЛЏбЇЗНГЬЪНЮЊ ЁЃ
ЃЈ2ЃЉвЊДгзАжУЂђжаЛёЕУвбЮіГіЕФОЇЬхЃЌПЩВЩШЁЕФЗжРыЗНЗЈЪЧ ЁЃ
ЃЈ3ЃЉзАжУЂѓгУгкДІРэЮВЦјЃЌПЩбЁгУЕФзюКЯРэзАжУ(МаГжвЧЦївбТдШЅ)ЮЊ (ЬюађКХ)ЁЃ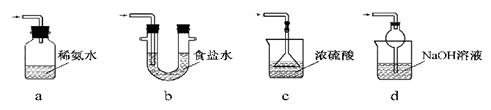
ЪЕбщЖў НЙбЧСђЫсФЦЕФаджЪ
Na2S2O5ШмгкЫЎМДЩњГЩNaHSO3ЁЃ
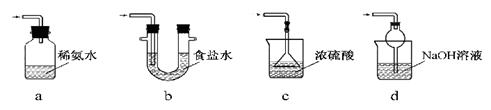
ЃЈ4ЃЉжЄУїNaHSO3ШмвКжаHSO3Ѓ ЕФЕчРыГЬЖШДѓгкЫЎНтГЬЖШЃЌПЩВЩгУЕФЪЕбщЗНЗЈЪЧ (ЬюађКХ)ЁЃ
aЃЎВтЖЈШмвКЕФpH bЃЎМгШыBa(OH)2ШмвК cЃЎМгШыбЮЫс
dЃЎМгШыЦЗКьШмвК eЃЎгУРЖЩЋЪЏШяЪджНМьВт
ЃЈ5ЃЉМьбщNa2S2O5ОЇЬхдкПеЦјжавбБЛбѕЛЏЕФЪЕбщЗНАИЪЧ ЁЃ
ЪЕбщШ§ ЦЯЬбОЦжаПЙбѕЛЏМСВаСєСПЕФВтЖЈ
ЃЈ6ЃЉЦЯЬбОЦГЃгУNa2S2O5зїПЙбѕЛЏМСЁЃВтЖЈФГЦЯЬбОЦжаПЙбѕЛЏМСЕФВаСєСП(вдгЮРыSO2МЦЫу)ЕФЗНАИШчЯТЃК
(вбжЊЃКЕЮЖЈЪБЗДгІЕФЛЏбЇЗНГЬЪНЮЊSO2ЃЋI2ЃЋ2H2OЃНH2SO4ЃЋ2HI)
ЂйАДЩЯЪіЗНАИЪЕбщЃЌЯћКФБъзМI2ШмвК25.00 mLЃЌИУДЮЪЕбщВтЕУбљЦЗжаПЙбѕЛЏМСЕФВаСєСП(вдгЮРыSO2МЦЫу)ЮЊ gЁЄLЃ1ЁЃ
ЂкдкЩЯЪіЪЕбщЙ§ГЬжаЃЌШєгаВПЗжHIБЛПеЦјбѕЛЏЃЌдђВтЕУНсЙћ (ЬюЁАЦЋИпЁБЁАЦЋЕЭЁБЛђЁАВЛБфЁБ)ЁЃ

ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com