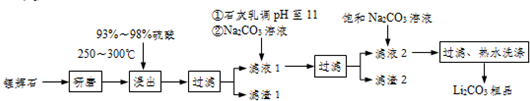
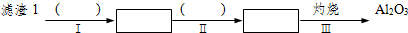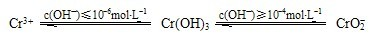(2010?西城区一模)工业上以锂辉石(Li
2O?Al
2O
3?4SiO
2,含少量Ca、Mg元素)为原料生产碳酸锂.其部分工艺流程如下:

已知:①Li
2O?Al
2O
3?4SiO
2+H
2SO
4(浓)
Li
2SO
4+Al
2O
3?4SiO
2?H
2O↓
②某些物质的溶解度(S)如下表所示.
| T/℃ |
20 |
40 |
60 |
80 |
| S(Li2CO3)/g |
1.33 |
1.17 |
1.01 |
0.85 |
| S(Li2SO4)/g |
34.2 |
32.8 |
31.9 |
30.7 |
(1)从滤渣1中分离出Al
2O
3的部分流程如下图所示,括号表示加入的试剂,方框表示所得到的物质.则步骤Ⅱ中反应的离子方程式是
Al3++3NH3?H2O=Al(OH)3↓+3NH4+
Al3++3NH3?H2O=Al(OH)3↓+3NH4+
.

(2)已知滤渣2的主要成分有Mg(OH)
2和CaCO
3.向滤液1中加入石灰乳的作用是(运用化学平衡原理简述)
增加Ca2+、OH-的浓度,有利于Mg(OH)2、CaCO3的析出
增加Ca2+、OH-的浓度,有利于Mg(OH)2、CaCO3的析出
.
(3)向滤液2中加入饱和Na
2CO
3溶液,过滤后,用“热水洗涤”的原因是
Li2CO3的溶解度随温度升高而减小,热水洗涤可减少Li2CO3的损失
Li2CO3的溶解度随温度升高而减小,热水洗涤可减少Li2CO3的损失
.
(4)工业上,将Li
2CO
3粗品制备成高纯Li
2CO
3的部分工艺如下.
a.将Li
2CO
3溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择透过膜隔开,用惰性电极电解.
b.电解后向LiOH溶液中加入过量NH
4HCO
3溶液,过滤、烘干得高纯Li
2CO
3.
①a中,阳极的电极反应式是
2C1--2e-=Cl2↑
2C1--2e-=Cl2↑
.
②b中,生成Li
2CO
3反应的化学方程式是
2Li2OH+NH4HCO3=Li2CO3+NH3+2H2O
2Li2OH+NH4HCO3=Li2CO3+NH3+2H2O
.