
题目列表(包括答案和解析)
某同学在一只烧杯里装有a g纯铁粉,加入200 mL 6 mol/L硝酸恰好完全溶解铁粉(假设还原产物只有NO).请完成对产物中铁元素价态的探究:
(1)提出合理假设:
假设1:产物只有+2价铁;
假设2:________;
假设3:________.
(2)设计实验:分别取反应后溶液装入两支试管甲、乙,在甲试管中滴加酸性高锰酸钾溶液;在乙试管中滴加KSCN溶液,观察现象.
推测实验现象与结论:①若现象为:________,
则假设1正确;②若现象为:________,
则假设2正确;③若现象为:________,
则假设3正确.
(3)a值范围为________.
(16分)(一)某同学在一只烧杯里装入一定量的纯铁粉,加入200mL 6mol/L的硝酸,铁粉恰好溶解,请探究产物中铁元素价态:
(1)提出假设:
假设1:产物只有+2价铁;
假设2:___________________________________;
假设3:___________________________________。
(2)设计实验:取反应所得溶液分别装入甲、乙两支试管,在甲中滴加酸性KMnO4溶液;在乙中滴加KSCN溶液,观察现象,推测实验现象与结论:
①若现象为____________________,则假设1正确;
②若现象为____________________,则假设2正确;
③若现象为____________________,则假设3正确。
(二)、氯化铁是常见的水处理剂,工业上制备无水FeCl3的流程为:

(3)吸收剂X为FeCl2溶液,其与尾气Cl2反应的离子方程式__________________。
(4)称取上述样品m克溶于25mL稀盐酸,用蒸馏水配成50mL溶液,加入稍过量的KI溶液充分反应: ,用淀粉作指示剂,用
,用淀粉作指示剂,用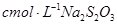 溶液进行滴定
溶液进行滴定 ,消耗Na2S2O3溶液VmL,则样品中FeCl3的质量分数为____。(相对原子质量Fe:56 Cl:35.5)
,消耗Na2S2O3溶液VmL,则样品中FeCl3的质量分数为____。(相对原子质量Fe:56 Cl:35.5)
(5)用FeCl3溶液(32%-35%)腐蚀铜板电路时所得废液含FeCl3、FeCl2和CuCl2,若用化学方法回收废液中的铜,简述操作要点:___________________________________________________。
(16分)(一)某同学在一只烧杯里装入一定量的纯铁粉,加入200mL 6mol/L的硝酸,铁粉恰好溶解,请探究产物中铁元素价态:
(1)提出假设:
假设1:产物只有+2价铁;
假设2:___________________________________;
假设3:___________________________________。
(2)设计实验:取反应所得溶液分别装入甲、乙两支试管,在甲中滴加酸性KMnO4溶液;在乙中滴加KSCN溶液,观察现象,推测实验现象与结论:
①若现象为____________________,则假设1正确;
②若现象为____________________,则假设2正确;
③若现象为____________________,则假设3正确。
(二)、氯化铁是常见的水处理剂,工业上制备无水FeCl3的流程为: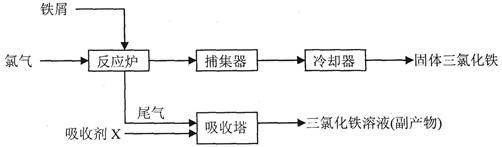
(3)吸收剂X为FeCl2溶液,其与尾气Cl2反应的离子方程式__________________。
(4)称取上述样品m克溶于25mL稀盐酸,用蒸馏水配成50mL溶液,加入稍过量的KI溶液充分反应: ,用淀粉作指示剂,用
,用淀粉作指示剂,用 溶液进行滴定
溶液进行滴定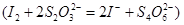 ,消耗Na2S2O3溶液VmL,则样品中FeCl3的质量分数为____。(相对原子质量Fe:56 Cl:35.5)
,消耗Na2S2O3溶液VmL,则样品中FeCl3的质量分数为____。(相对原子质量Fe:56 Cl:35.5)
(5)用FeCl3溶液(32%-35%)腐蚀铜板电路时所得废液含FeCl3、FeCl2和CuCl2,若用化学方法回收废液中的铜,简述操作要点:___________________________________________________。
在托盘天平两端各放一只烧杯, 调节至平衡. 向两烧杯里分别注入等质量、 等溶质质量分数且过量的稀硫酸, 然后在一只烧杯里加入一定质量的镁, 在另 一烧杯里加入等质量的铜铝合金, 两烧杯的反应完成后, 天平仍保持平衡. 则 铜铝合金中铜与铝的质量比为
[ ]
A. 1:3 B. 1:2 C. 3:4 D. 2:3
| 观察要点或实验步骤 | 现象、结论或注意事项 | |
| 方法一 | 观察二者外观上的细小差别 | 呈 白色粉末 白色粉末 状的是碳酸钠,呈白色细小晶体 白色细小晶体 的是碳酸氢钠 |
| 方法二 | 分别滴入几滴水 | 结成块状并且试管底部温度较高的是 碳酸钠 碳酸钠 ;未结块并且试管底部温度较低的是 碳酸氢钠 碳酸氢钠 . |
| 方法三 | 再分别加入10mL水,滴入 1~2滴酚酞试液 |
该操作中加入水后应 用力振荡或用玻璃棒搅拌 用力振荡或用玻璃棒搅拌 ;滴入酚酞后应着重观察 所得溶液颜色的深浅 所得溶液颜色的深浅 . |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com