
题目列表(包括答案和解析)
| ||
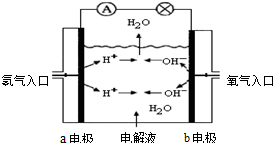 图为氢氧燃料电池原理示意图,按照此图的提示,回答以下问题:
图为氢氧燃料电池原理示意图,按照此图的提示,回答以下问题:水的电离平衡为H2O  H+﹢OH-,△H>0,下列叙述不正确的是
H+﹢OH-,△H>0,下列叙述不正确的是
A.将水加热,pH减小
B.恒温下,向水中加入少量固体KOH,Kw不变
C.向水中滴入稀醋酸,c(H+)增大
D.向水中加入少量固体NaClO,平衡逆向移动
从化学角度分析,下列叙述不正确的是:
| A.化学是在分子原子水平上认识物质,所以通过化学手段可以识别、改造和创造分子 |
| B.化学是以实验为基础的一门学科,定量研究方法是化学发展为一门学科的重要标志 |
| C.绿色化学是指以绿色植物为原料来源的现代新型化学工业 |
| D.化学反应中的能量变化常用焓变(△H)来表示,△H=H(反应产物)-H(反应物) |
下列叙述不正确的是:
A.根据金属活动性顺序,可以推断冶炼金属时可能的方法
B.根据元素周期表中元素的位置,可以寻找合适的半导体材料
C.根据元素某种原子的质子数和中子数,可以确定该元素的相对原子质量
D.根据酸、碱、盐的溶解性表,可以判断某些溶液中的复分解反应能否进行
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com