
题目列表(包括答案和解析)
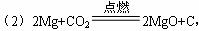
(1)写出下列物质的化学式,A_________________;C__________________;E_____________;H________________。
(2)写出A+N,C+H2O的化学方程式:?________________________________________。
(3)写出H的水溶液与D反应的离子方程式:?______________________________________。
(4)写出A单质与热水反应的化学方程式:?________________________________________。
A、B、C、D、E、F、M、N、X、Y是中学化学中常见的物质,其中A、B、C、D、E、F是化合物,M、N、X、Y是单质。已知反应关系如下图所示(部分产物已略去):
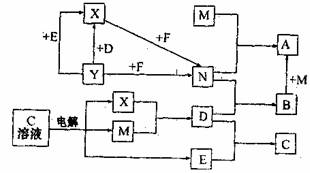
(1)向沸腾的蒸馏水中滴加A的饱和溶液,可以得到红褐色液体。A的化学式是
。
(2)将NaOH溶液注入新B溶液中,观察到的现象是 (选填序号)。
①生成白色沉淀
②生成血红色沉淀
③生成红褐色沉淀
④生成蓝色沉淀
⑤生成白色沉淀后,迅速变成灰绿色沉淀,最后变成红褐色沉淀
(3)C溶液电解的离子方程式是 。
(4)化合物F中含有组成单质N的元素,且该元素质量分数为70%。化合物F和单质Y反应的化学方程式是 。
(5)组成单质N的元素和碳的合金在潮湿的空气中容易腐蚀。发生腐蚀时,正极的电极反应式是 。
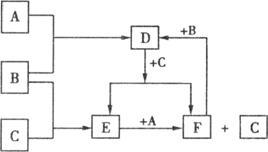
请回答下列问题:
(1)A、B、C三种单质的化学式(分子式)分别是A__________:B________C________,其中A、C单质的晶体类型属于________________。
(2)B与C反应生成E时观察到的现象是________________________________________。
(3)D和C反应生成E和F的离子方程式:________________________。
(4)在测定C的硫酸盐晶体结晶水含量实验中。若坩埚质量为m,坩埚与C的硫酸盐晶体总质量为m1,加热后称量坩埚与C的无水硫酸盐总质量为m2,则晶体中结晶水的质量分数ω=________(写计算式)。如果实验中加热温度过高致使固体出现黑色,则测定结果________(填“偏高”“偏低”“不变”)。
(12分)已知:A、B、C为中学常见的单质,A为淡黄色固体;D、E、F为中学常见的氧化物,E是具有磁性的黑色晶体;H、K为中学常见的盐;M为一种常见的无色液体。各物质间的转化关系如下图所示(某些条件已略去)。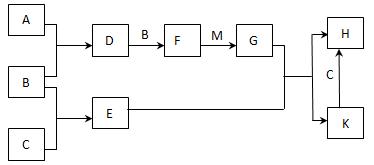
请回答:
(1)物质K的化学式为 。
(2)物质M的电子式为 。
(3)D可使酸性KMnO4溶液褪色,体现了D物质的 (填字母序号)。
A. 氧化性 B. 还原性 C. 漂白性
(4)C与M在一定条件下反应的化学方程式为 。
(5)先将D气体通入BaCl2溶液中,再通入NH3,实验过程中的现象为 。
(6)H溶液在空气中常期放置会出现红褐色浑浊,请用一个离子方程式表示其变化的原因: 。
(7)A与C可以在一定条件下发生化合反应,其产物中元素A与C的质量比为4:7,该物质是某矿石的主要成分之一,常用于生产G。某化工厂所用矿石样品含杂质25%,若取8.8吨该矿石,假设生产过程中无其他损失,可制得含G 98%的产品 吨。
已知:A、B、C为中学常见的单质,A为淡黄色固体;D、E、F、M为中学常见的氧化物,E是磁铁矿的主要成分(是黑色固体);H、K为中学常见的盐;M是一种常见的无色液体。各物质间的转化关系如下图所示(某些条件已略去)。
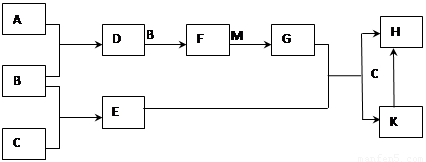
请回答:
(1)物质H的化学式为 。
(2)由F与M作用生成G的化学反应基本类型为 。
(3)A与C在加热条件下反应的化学方程式为: 。
(4)G的浓溶液在加热条件下能跟C反应,该反应中G体现了 (填序号)。
A.氧化性 B.还原性 C.漂白性 D.酸性
(5)若先将D气体通入BaCl2溶液中,再通入NH3,实验过程中的现象为 。
(6)H溶液在空气中长期放置会出现红褐色浑浊,请用一个离子方程式表示其变化的原因: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com