下表为元素周期表的一部,请参照元素①-⑩在表中的位置,用化学用语回答下列问题:
| 族周期 |
IA |
|
0 |
| 1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
| 2 |
|
② |
|
③ |
④ |
|
⑤ |
|
| 3 |
⑥ |
⑦ |
⑧ |
⑨ |
|
|
⑩ |
|
(1)请写出②的元素符号
Be
Be
(2)请写出③的最高价氧化物的电子式
.
(3)比较⑤、⑥、⑧的原子半径由大到小的顺序为(用元素符号表示)
Na>Al>F
Na>Al>F
(4)比较③、④、⑨的最高价含氧酸的酸性由强到弱的顺序是(用酸的化学式表示)
HNO3>H2CO3>H2SiO3(或H4SiO4)
HNO3>H2CO3>H2SiO3(或H4SiO4)
.
(5)写出在元素①-⑩中最高价氧化物对应水化物的最强碱与最强含氧酸之间的化学反应方程式
NaOH+HClO4═NaClO4+H2O
NaOH+HClO4═NaClO4+H2O
(6)⑦⑧两元素相比较,金属性较强的是
镁
镁
(填名称),可以验证该结论的实验是
(b)(c)
(b)(c)
(填编号).
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将形状、大小相同的这两种元素的单质分别和同浓度的盐酸反应
(c)将形状、大小相同这两种元素的单质分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性.



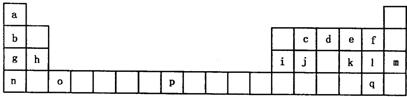
 下表是元素周期表的前三周期:
下表是元素周期表的前三周期: