
题目列表(包括答案和解析)




近几年我国某些城市酸雨污染较为严重,主要是因为大量燃烧含硫量高的煤而形成的,此外,各种机动车排放的尾气也是形成酸雨的重要原因。
【提出问题】通过实验证明煤中含有碳元素和硫元素。
【查阅资料】
(1)“二氧化硫能使高锰酸钾溶液褪色(由紫红色变为无色)请完成该反应的化学方程式
SO2 + KMnO4 + H2O= K2SO4 + MnSO4 + H2SO4
根据上述资料,甲、乙、丙三位同学分别设计实验方案进行探究。
【实验探究】
甲同学:
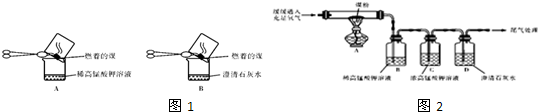
“实验操作”:甲同学进行了如下图所示A、B两步实验:

“实验现象”: A中稀高锰酸钾溶液褪色,B中澄清石灰水变浑浊。
“得出结论”:煤燃烧生成二氧化硫和二氧化碳,证明煤中含有碳元素和硫元素。
(2)乙同学认为甲同学的实验方案不合理,其理由是: 。
丙同学:
“实验操作”:丙同学进行了如下图所示实验(部分装置在图中略去):

【探究与结论】
(3)上图C装置的作用是 。
(4)要证明煤中含有碳元素和硫元素的现象 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com