|
实验室常用间接碘量法测定胆矾中铜含量.
实验原理
在弱酸性条件下,Cu2+与I-作用可生成I2,并被还原成白色的碘化亚铜沉淀;I2溶于过量的KI溶液中:I2+I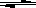 I3-,可用Na2S2O3标准溶液滴定,其反应为:2S2O32-+I3-=S4O62-+3I-. I3-,可用Na2S2O3标准溶液滴定,其反应为:2S2O32-+I3-=S4O62-+3I-.
实验步骤
第一步:准确称取ag含少量Fe2(SO4)3胆矾试样.
第二步:将试样置于250mL碘量瓶(带磨口塞的锥形瓶)中,加50mL蒸馏水、5mL 3mol/LH2SO4溶液,振荡,得到澄清、透明溶液.
第三步:向第二步得到的溶液中先加少量NaF溶液,再加入足量的10%KI溶液,摇匀.
第四步:盖上碘量瓶瓶盖,置于暗处5min,充分反应后,加入淀粉溶液作指示剂.
第五步:将cmol/LNa2S2O3标准溶液装入滴定管.
第六步:滴定,当碘量瓶中溶液由蓝色变为无色且在半分钟内不再变化时,共用去VmL标准溶液.
资料卡片
氧化性:O2>Fe3+>Cu2+>I2>FeF63-.
讨论下列问题:
| 
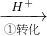 Cr2O72-
Cr2O72-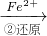 Cr3+
Cr3+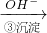 Cr(OH)3↓
Cr(OH)3↓ Cr2O72-
Cr2O72- Cr3+
Cr3+ Cr(OH)3↓
Cr(OH)3↓