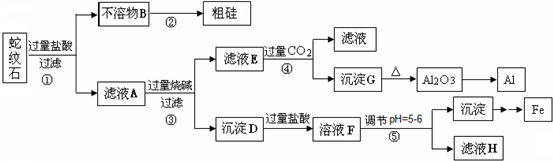
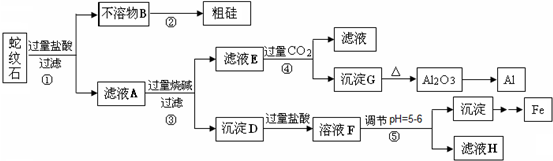
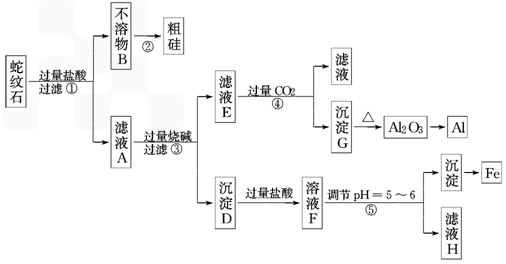
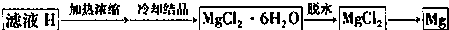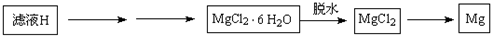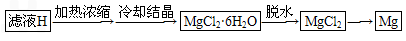蛇纹石矿可以看作由MgO、Fe
2O
3、Al
2O
3和SiO
2组成.某实验小组设计如下流程欲分别制得单质Al、Fe、Mg和Si.

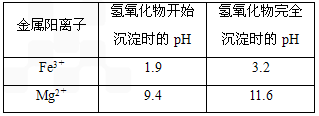
有关氢氧化物沉淀的pH见下表:
| 金属阳离子 |
氢氧化物开始沉淀时的pH |
氢氧化物完全沉淀时的pH |
| Fe3+ |
1.9 |
3.2 |
| Mg2+ |
9.4 |
11.6 |
(1)写出不溶物B在生产中的一种用途:
光导纤维
光导纤维
.
(2)操作④中滤液E与过量CO
2反应生成沉淀G的离子方程式为:
AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
.
(3)操作⑤中调节pH到5~6时,可以用到的试剂(填序号)
cd
cd
.
a. NaOH溶液 b.氨水 c. Fe
2O
3 d. Mg(OH)
2(4)从滤液H制取金属Mg的流程如下:

Ⅰ.流程中由滤液H中得到MgCl
2?6H
2O的方法是
加热浓缩
加热浓缩
、
冷却结晶
冷却结晶
、过滤、洗涤;
Ⅱ.在干燥的HCl气流中加热MgCl
2?6H
2O制取无水氯化镁的原因是
Mg2++2H2O?Mg(OH)2+2H+,通入HCl,使C(H+)增大,抑制Mg2+的水解成Mg(OH)2,确保生成MgCl2
Mg2++2H2O?Mg(OH)2+2H+,通入HCl,使C(H+)增大,抑制Mg2+的水解成Mg(OH)2,确保生成MgCl2
.(应用离子方程式和简要文字说明)
Ⅲ.冶炼镁的方法用化学方程式表示为
.