下表是某城市某日的空气质量报告:
| 污染指数 |
首要污染物 |
空气质量等级 |
空气质量状况 |
| 55 |
SO2 |
Ⅱ |
良 |
该市某校研究性学习小组对表中首要污染物SO
2导致酸雨的成因进行了如下探究:
(1)用如图所示装置进行实验.

①A装置的作用是
(填“干燥”或“氧化”)SO
2气体.
②实验过程中,B装置内石蕊试纸的颜色没有发生变化,C装置内湿润的蓝色石蕊试纸变
色,说明SO
2与水反应生成一种酸.
③D装置的作用是
.D中发生反应的化学方程式是
.
(2)往盛有水的烧杯中通入SO
2气体,测得所得溶液的pH
7(填“>”“=”或“<”),然后每隔1h测定其pH,发现pH逐渐
(填“变大”或“变小”),直至恒定.说明烧杯中的溶液被空气中的氧气氧化最终生成H
2SO
4.
(3)SO
2形成酸雨的另一途径为:SO
2与空气中的O
2在飘尘的作用下反应生成SO
3,SO
3溶于降水生成H
2SO
4,则在此过程中的飘尘是作为
(填“催化剂’’或“氧化剂”).
(4)SO
2与空气中的氧气、水反应生成硫酸而形成酸雨.该市可能易出现酸雨.
(5)汽车排放的尾气,硝酸、化肥等工业生产排出的废气中都含有氮的氧化物,氮的氧化物溶于水最终转化为
,是造成酸雨的另一主要原因.

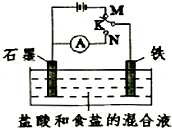 (2013?日照二模)用如图所示装置进行实验,下列叙述不正确的是( )
(2013?日照二模)用如图所示装置进行实验,下列叙述不正确的是( )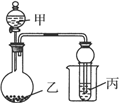 用如图所示装置进行实验,将少量液体甲逐滴加入到固体乙中,试管中试剂为丙,则下表中现象与结论均正确的是( )
用如图所示装置进行实验,将少量液体甲逐滴加入到固体乙中,试管中试剂为丙,则下表中现象与结论均正确的是( )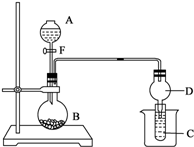 用如图所示装置进行实验,将液体A逐滴加入到固体B中,回答下列问题:
用如图所示装置进行实验,将液体A逐滴加入到固体B中,回答下列问题: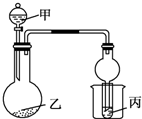 用如图所示装置进行实验,将少量液体甲逐滴加入到固体乙中(可加热),试管中试剂为丙,则下表中对应选项错误的是( )
用如图所示装置进行实验,将少量液体甲逐滴加入到固体乙中(可加热),试管中试剂为丙,则下表中对应选项错误的是( )