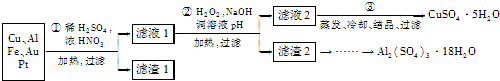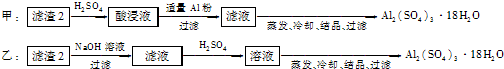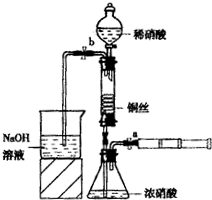
(2011?朝阳区二模)某同学利用下面装置实现铜与浓、稀硝酸反应,过程如下:
Ⅰ、取一段铜丝,用稀硫酸除去铜锈〔主要成分是 Cu
2(OH)
2CO
3〕
Ⅱ、将洗涤后的铜丝做成匝数很多的螺旋状
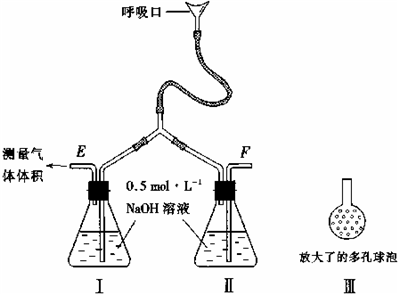
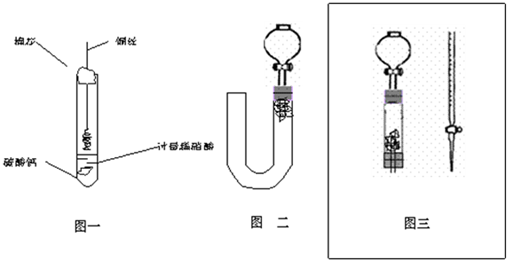
Ⅲ、按如图所示连接仪器、检查气密性、装入化学试剂
(1)过程Ⅰ发生反应的离子方程式是
Cu2(OH)2CO3+4H+=2Cu2++CO2↑+3H2O
Cu2(OH)2CO3+4H+=2Cu2++CO2↑+3H2O
;
(2)过程Ⅱ将铜丝做成螺旋状的目的是
增大铜丝与酸的接触面积,提高化学反应速率
增大铜丝与酸的接触面积,提高化学反应速率
;
(3)过程Ⅲ的后续操作如下:
①为使浓硝酸与铜丝接触,操作是
打开止水夹a和b,从注射器中推入空气
打开止水夹a和b,从注射器中推入空气
.当红棕色气体较多时,轻抽注射器使反应停止,关闭a,取下注射器.生成红棕色气体的化学方程式是
Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O
Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O
.
②控制b和分液漏斗活塞,玻璃管充满稀硝酸时,关闭b打开a,可见无色气体.稀硝酸充满玻璃管的实验目的是
将玻璃管中的NO2排出
将玻璃管中的NO2排出
.
(4)将3支盛满红棕色气体的小试管分别倒置在盛有常温水、热水和冰水的3只烧杯中,发现液面上升的高度明显不一致.结果如下表所示:
| 实验编号 |
水温/0C |
液面上升高度 |
| 1 |
25 |
超过试管 |
| 2 |
50 |
不足试管 |
| 3 |
0 |
液面上升超过实验1 |
①根据上表得出的结论是
温度越低,进入试管中的溶液体积越多
温度越低,进入试管中的溶液体积越多
;
②查阅资料:
a.NO
2与水反应的实际过程为:2NO
2+H
2O═HNO
2+HNO
3 3HNO
2═HNO
3+2NO↑+H
2O
b.HNO
2不稳定.
产生上述现象的原因是
温度低,HNO2分解量减少,分解产生的NO气体量减少,且生成的NO所占体积小,所以进入试管中的溶液体积增大
温度低,HNO2分解量减少,分解产生的NO气体量减少,且生成的NO所占体积小,所以进入试管中的溶液体积增大
.

 (2011?朝阳区二模)某同学利用下面装置实现铜与浓、稀硝酸反应,过程如下:
(2011?朝阳区二模)某同学利用下面装置实现铜与浓、稀硝酸反应,过程如下: