
题目列表(包括答案和解析)
有A、B、C三种金属,将A放入B的硝酸盐溶液中,A的表面有B析出,而将A、B、C分别置于稀硫酸中,只有C可溶于硫酸并放出氢气,则A、B、C三种金属的活动性顺序为
[ ]
有A、B、C三种金属,将A放入B的硝酸盐溶液中,A的表面有B析出,而将A、B、C分别置于稀硫酸中,只有C可溶于硫酸并放出氢气,则A、B、C三种金属的活动性顺序为
[ ]
 将A、B、C和锌四种金属分别同时放入稀盐酸中,小明将观察到的现象形象的画了一幅卡通画,每个卡通人物表示一种金属,周围的小黑点表示反应中生成的气体.问:
将A、B、C和锌四种金属分别同时放入稀盐酸中,小明将观察到的现象形象的画了一幅卡通画,每个卡通人物表示一种金属,周围的小黑点表示反应中生成的气体.问: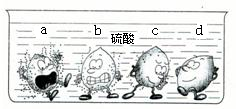 学过金属的活动性顺序以后,明明同学对其一系列知识进行了研究.
学过金属的活动性顺序以后,明明同学对其一系列知识进行了研究.| X盐溶液 | Y盐溶液 | Z盐溶液 | |
| Ni | 无 | 无 | 有 |
| Mn | 无 | 有 | 有 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com