
题目列表(包括答案和解析)
50、人类的生产活动离不开金属,下列三种金属被发现使用的先后顺序依次为:铜、铁、铝。
(1)金属大规模被使用的先后顺序跟 有关
①金属的导电性 ②地壳中金属元素的含量 ③金属的活动性
(2)为探究金属Mg、Fe、Mn的活动性,在相同温度下,取大小相同、表面光亮的三种金属薄片分别投入等体积、等浓度的足量稀盐酸中(反应中Mn显+2价),请回答:
|
金属 |
Mg |
Fe |
Mn |
|
反应现象 |
放出气泡速率很快 |
放出气泡速率很慢 |
放出气泡速率较快 |
|
结论 |
三种金属的活动性: > > |
(3)写出上述任一条反应方程式:
(4)除了用上述方法外,请你再设计一种方法证明三者的活动性:(药品自选,纯净的Mn是一种银灰色的金属)
|
验证方法 |
现象与结论 |
|
|
|
49、有一包混合物,其中可能含有适量的碳酸钙、碳粉、氧化铜、氧化铁中的一种或几种。现做如下实验:
①取样,加热到高温,产生一种无色气体,该气体能使澄清的石灰水变混浊。②把足量的稀盐酸滴入冷却后的固体残渣中,残存固体全部溶解,同时产生一种可燃性气体,该混合物的中一定有 ,一定没有 。
48、30℃时,NaOH溶解于水的实验数据如下表。
|
实验序号 |
水的质量(克) |
加入NaOH质量(克) |
所得溶液质量(克) |
|
① |
10 |
5 |
15 |
|
② |
10 |
10 |
20 |
|
③ |
10 |
15 |
21 |
|
④ |
10 |
20 |
21 |
(1)实验①中,溶液的质量分数为 。
(2)实验②所得的溶液是 溶液(填饱和或不饱和)。
(3)30℃时,NaOH的溶解度为 克/100克水
(4)如果在实验②中,滴加足量的硫酸铜溶液,则会生成 mol沉淀,该反应的化学方程式 。
47、碳、氢、氧是与人类密切相关的三种元素,它们可以组成很多不同的物质,请根据要求完成与它们相关的试题。
(1)请写出相关物质的化学式
①式量最小的氧化物 ,②可导致温室效应的气体 ,③自然界最硬的单质 ,④可供呼吸的气体 ,⑤具有可燃性的气体 。
(2)兴奋剂检测是运动员的一项重要检测,诺龙是兴奋剂中的一种,其化学式是C18H26O2,它由 种元素组成,其中原子个数比是 ,1mol诺龙中含氧原子 mol。
(3)一般情况下,二氧化碳不燃烧也不支持燃烧,通常可以用来灭火。金属镁却可以在二氧化碳中燃烧,燃烧的化学方程式为: 。在该反应中,镁作 剂。
46、某无色气体可能含有CO2、CO、H2中的一种或几种,依次进行以下实验(假设每步反应均完全进行):①通过炽热的炭层后,恢复到原状态,气体体积不变;②通过灼热的氧化铜时,粉末变成红色;③通过白色硫酸铜粉末时,粉末变成了蓝色晶体;④通入澄清石灰水,石灰水变浑浊。下列判断正确的是…………………………………( )
A、原混合气体中一定含有CO2、CO和H2
B、原混合气体中一定含有H2、CO,一定没有CO2
C、原混合气体中一定含有H2、CO,可能含有CO2
D、原混合气体中一定含有H2、CO2,可能含有CO
45、X是某种金属,在化合物中显+2价,相同质量的X和Mg与足量同浓度的酸反应,产生气体与时间的关系如图所示,由此不能得到的结论是…………………………( )
 A、Mg的活动性比X强
A、Mg的活动性比X强
B、产生相同质量的氢气需要的X更多
C、相同质量的金属与酸反应生成的气体Mg可能比X少
D、相同质量的金属与酸反应生成的气体Mg可能和X一样多
44、下列物质中,可用于鉴别澄清石灰水与氢氧化钠溶液的试剂是……………………( )
A、酚酞试液 B、紫色石蕊试液 C、盐酸 D、碳酸钠溶液
43、下列产物可以由金属直接与酸反应而制得的是……………………………………( )
A、FeCl3 B、FeSO4 C、CuSO4 D、AgCl
42、常温常压下,50mL某气态物质含有1.34×1021个分子,而在这些分子里又含有4.02×1021个原子,则判断该物质是一种………………………………………………………( )
A、单质 B、化合物
C、混合物 D、以上都有可能
41、工业上常用乙炔燃烧产生的高温火焰来切割金属。若用R表示乙炔,其燃烧的化学方程式为:2R + 5O2 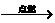 4CO2 + 2H2O ,则乙炔的化学式为
……………………………( )
4CO2 + 2H2O ,则乙炔的化学式为
……………………………( )
A、C2H2 B、C2H4 C、CH3COOH D、C2H6
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com