
题目列表(包括答案和解析)
7.下列符号既表示一种元素,又表示该元素的一个原子,还能表示该元素形成的单质是( )
A.Cl B. Ag C. O2 D. 2O2
6.经分析,某种物质只含有一种元素,则该物质不可能是 ( )
A.混合物 B.纯净物 C.单质 D.化合物
5.某微粒结构示意图为+X2 8 Y。其中___________决定元素种类,__________决定元素的化学性质。当x=________时,表示原子;当x________时,表示阳离子;当x________时,表示阴离子。
4.元素是具有______________________________________的总称。
A.元素具有宏观概念,只有______________,没有_________________。
 B.元素符号表示的意义,①表示________________,②表示________________。
B.元素符号表示的意义,①表示________________,②表示________________。
3.构成物质的微粒有________________________。
A.分子和原子的主要区别是_____________________________,分子由____________构成,但分子_________比原子大。
B.原子不显电性。因为____________的原子核和_____________核外电子,二者所带的______相等,______相反。因此在原子中有两组等量关系:核电荷数=__________=___________;相对原子质量= _______ + ________。
C.离子是由原子_______________形成,失去电子带___________电,形成_____________;得到电子带_________,形成________。
D.用化学符号填空;
汞原子_______铝原子________氯原子_______过氧化氢分子_______ 硫酸分子_______
亚硫酸分子_______硫化氢分子________硫酸根离子_______硫离子_______铝离子_________氢离子______碳酸根离子_______硝酸根离子_______氢氧根离子________铵根离子________锰酸根离子______亚铁离子__________铁离子________磷酸根离子_______镁离子__________
银离子_________高锰酸根离子___________硫酸铁___________硫酸亚铁_____________
2.用微粒的观点解释下列现象:
①相同质量的CO2气体体积比干冰体积大_________________________________________;
②一氧化碳可以作燃料,而二氧化碳可以用作灭火剂________________________________;
③漫步在花园里可以闻到花香___________________________________________________;
④一个氢分子质量为3.34×10-27kg_______________________________________________;
⑤湿衣服晾在阳光下比在室内更容易干___________________________________________;
⑥液氧和氧气状态不同,但却具有相同的化学性质__________________________________;
⑦铺铁轨时,在衔接处要留有缝隙________________________________________________;
⑧水在通电条件下分解为氢气和氧气_____________________________________________;⑨用打气筒将空气压入足球内_________________________________________________。
1.不同的物质有不同的性质,是因为不同的物质由_______________的微粒构成。
(二)对废液作探究性实验
(4)取少量废液,向废液中加入BaCl2溶液,没有产生沉淀,继续加入Ba(OH)2溶液产生白色沉淀,过滤,得沉淀X和滤液Y,向沉淀X中加入足量稀盐酸,沉淀全部消失,没有气泡,向滤液Y中加入少量AgNO3溶液,产生白色沉淀,加稀HNO3沉淀不消失,则原废液中可能含______、_______、______。
5.有一包固体物质,可能含有CuSO4、KCl、Na2CO3、NaNO3、Na2SO4、BaCl2中一种或几种:
(1)取少量样品,加入适量水搅拌,得无色溶液;
(2)向所得溶液中加入BaCl2溶液,有白色沉淀生成,过滤;
(3)向滤液中加入足量稀HNO3,再滴入AgNO3溶液,有白色沉淀生成;
(4)向实验(2)所得滤渣中加入足量稀HNO3,沉淀部分溶解并放出无色气体。则原固体中一定含_________________,一定不含________________,另外不能确定的物质有哪几种可能的组成?_________________________________________________________。
6.已知某一无色溶液由H2SO4、HNO3、K2CO3、CuSO4、K2SO4、KNO3、NaCl七种溶液中的两种混合而成,现进行如下实验:
(1)向混合溶液中滴入紫色石蕊试液,溶液呈红色;
(2)向混合溶液中加入过量的硝酸钡溶液,产生白色沉淀,过滤;
(3)再向上述滤液中加入硝酸银溶液,无明显现象。
根据上述实验分析,此混合溶液中存在的溶质可能是:(有几种填几种,可不填满)
①________和_________;②_________和____________;③_________和____________; ④_________和_________;⑤_________和____________。
7.某白色固体可能含有CaCO3、(NH4)2SO4、BaSO4、NaCl、(NH4)2CO3中的一种或几种,现对该固体进行如下实验:

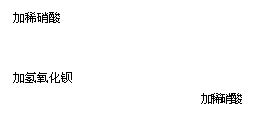
根据以上现象推断,此白色粉末一定含有________________,一定不含有___________,不能确定是否含有_____________________。
8.现有甲、乙、丙三种可溶性的正盐溶液,按下图实验,且甲与乙、乙与丙恰好完全反应。

试推断(写化学式或离子符号):溶液甲是___________,沉淀B是_____________,溶液乙是___________;沉淀F是_________,滤液E中的溶质是_____________________________。
9. 有一包白色固体A,可能含有FeCl3、CaCO3、NaOH、Ba(OH)2、BaCl2、Na2SO4中的几种,取少量A做如下实验,现象如图所示,试用化学式填空:
有一包白色固体A,可能含有FeCl3、CaCO3、NaOH、Ba(OH)2、BaCl2、Na2SO4中的几种,取少量A做如下实验,现象如图所示,试用化学式填空:
(1)白色沉淀B是______________;D是__________________;
(2)白色固体A中一定不存在的物质为____________________;
(3)若白色固体A中只含二种物质,它们是___________________________;
(4)白色固体A还有哪些可能的组成:①_____________________,②_______________,
③_____________________________,④__________________________。(可不填满)
10.
|

|
根据以上实验事实,用化学式回答:
(1)当废水溶液中仅含有一种溶质时,该溶质是________________;
(2)当废水溶液中含多种溶质时,除(1)中溶质外,还可能存在的盐是_________、________、__________,以及其它可能存在的溶质是_________、________。
11.有一包固体混合物,可能是Na2SO4、CaCO3、BaCl2、CuSO4、NaCl中的一种或几种组成,现做如下实验:
(1)将此固体充分溶解于水中,得到白色沉淀,上层为无色溶液;过滤后,在白色沉淀中滴加足量稀硝酸,未见沉淀溶解。由此可知,该混合物中一定有_____________,一定没有______________,可能有______________。
(2)为了确定“可能”存在的物质是否存在,现取原混合物3.5克,充分溶于水恰好完全反应后,过滤,将滤纸上的固体洗涤,烘干后,称量质量为2.33克,通过计算确定,“可能有”的物质__________________(填“存在”或“不存在”)。
12.有一种无色混合气体,可能含有H2、CO、HCl、CO2、N2中的一种或多种。现在该气体经下列处理(假设每步反应均完全),试回答下列问题:
无色混合气体→澄清石灰水(无沉淀,气体明显减少)→浓硫酸→灼热氧化铜(变红)→无水硫酸铜(变蓝)→NaOH溶液→浓硫酸→收集到少量气体
(1)经过澄清石灰水时,气体明显减少,说明原混合气体中一定含有________(填化学式); (2)无水硫酸铜变蓝说明原混合气体中一定含有__________(填化学式);
(3)综合上述实验现象,推测该混合气体成份可能是:(将所有情况写全、多写、错写倒扣分,若横线不够可另加)
第一种情况__________________________ ; 第二种情况__________________________;
第三种情况__________________________ ; 第四种情况__________________________。
13.某校初中化学课外小组学生,将一些可溶性化合物溶于水,配制成的甲、乙两瓶溶液,共含有H+、K+、Ag+、Ba2+、OH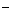 、Cl
、Cl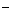 、NO
、NO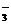 、CO
、CO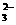 八种离子,每瓶溶液里含有四种离子各不相同。已知向甲瓶溶液里滴入紫色石蕊试液后,溶液变成蓝色。据此推测乙瓶溶液中的离子应该是_________________________________(填离子符号)。
八种离子,每瓶溶液里含有四种离子各不相同。已知向甲瓶溶液里滴入紫色石蕊试液后,溶液变成蓝色。据此推测乙瓶溶液中的离子应该是_________________________________(填离子符号)。
14.
|
|
 硝酸钾、氯化钡(均为溶液)8种溶液中选4种,
硝酸钾、氯化钡(均为溶液)8种溶液中选4种,
使各线条相连物质均能发生反应,且生成难溶物,
将选出物质的化学式按要求填入空格,并写出
|
|
 A_______ B______ C______ D______
A_______ B______ C______ D______
(1)________________________________; (2)_________________________________;
(3)__________________________________; (4)________________________________。
15.有A、B、C、D四瓶失去标签的白色粉末(均为纯净物),巳知它们可能是硫酸铜、碳酸
钙、氯化钾、硫酸钾中的一种。某学生的鉴别实验过程记录如下:
步骤1:A、B、C、D四种白色粉末各一药匙,分别放入四支洁净的试管中,各加蒸馏水2mL,振荡后处置。四支试管底部均有固体存在,只有盛放A的试管中液体呈蓝色,其他呈无色。
步骤2:继续向盛放B、C、D的试管中加入等量的稀硫酸,只有D的试管中有气泡产生,其他均无明显变化。
步骤3:将步骤2盛放B和C的试管中固体滤出后,向滤液中分别滴加氯化钡溶液。
请根据根据该学生的实验过程,回答下列问题:
(1) 步骤1中“四支试管底部均有固体存在”,与该学生预测的“只有一支试管中有固体存在,其他试管中均为澄清溶液”的现象不同,其原因可能是______________________________。
(2) 步骤3中,可能观察到的实验现象是_________________________________。
(3) 根据该学生的实验,请选择下列①或②中的一个问题回答:
①四种白色粉末均已一一鉴别出来,分别是____________________________(写代号及其对
应物质的化学式)。
②四种白色粉末只能部分被鉴别出来,分别是_______________________(写代号及其对应物质的化学式);对尚未鉴别出来的物质,请设计实验进行确定,并填写下表。
|
实验操作 |
实验现象及结论 |
|
|
|
16.为了除去食盐(主要成分为NaCl)样品中含有少量的氯化镁和硫酸钠杂质,某学生根据
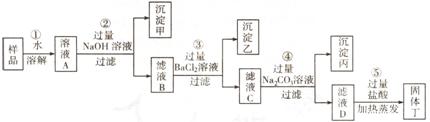
氯碱工业中精制食盐水的基本原理,运用所学知识设计了如下图所示的①至⑤步除杂方案:
请根据上述除杂方案,回答下列问题:
(l)沉淀甲是__________________; 滤液C中的溶质是____________________; 操作⑤中加入过量盐酸的作用是__________________。
(2)假设整个操作过程中物质转化无损失,则固体丁中NaCl的质量比原样品中的质量_____________(填增大、不变或减小);若在操作②中改为加过量的KOH溶液,固体丁中可能含有的杂质是_______________________________。
17.现有Cu、CuO、CuSO4、C、CO、CO2六种物质,它们的反应关系如下图所示(图中每个
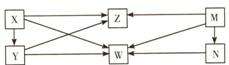 字母分别代表上述六种物质中的一种)。
字母分别代表上述六种物质中的一种)。
(1)请利用初中所学知识推断图中Y、Z、W、N分别对应物质的化学式:
Y____________、Z______________ 、
W____________、N______________;
(2)写出M→N的化学方程式____________________________________;
(3)写出X→W的化学方程式____________________________________。
18.某固体可能由Na2SO4、NaCl、Na2CO3、KNO3中的一种或几种组成,现进行如下实验:
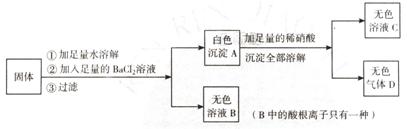 试回答:
试回答:
(1)白色沉淀A的化学式为________,无色气体D的化学式为_______________。
(2)原固体中一定含有___________,一定不含有_____________,可能含有_________。
(3)为检验上述可能含有的物质是否一定存在,某同学又设计了如下实验方案:①取少量固体溶于水,加入足量的Ba(NO3)2溶液,充分反应后,过滤;②取滤液加入AgNO3溶液,观察有无白色沉淀生成,由此得出结论。在上述某同学的实验方案①中,加入足量的Ba(NO3)2 溶液的目的是________________________________________________________。
19. 下图中的物质都是你在初中化学中见过的物质。除反应①外,其它反应的条件均已略去。
下图中的物质都是你在初中化学中见过的物质。除反应①外,其它反应的条件均已略去。
(1)写出反应①的化学方程式_________________________________;
(2)如果E为单质或者氧化物,D都是同种物质,则D的化学式为________________;如果E为单质或者酸,D都是同种物质,则D的化学式为______________;如果E为单质或者氧化物,F都是同种物质,则F的化学式为___________;
(3)当E为单质时,反应③的化学方程式为__________________(任写一个);
(4)当E为酸时,反应③可能属于_________(填字母序号)
A.化合反应 B.分解反应 C.复分解反应 D.置换反应
20.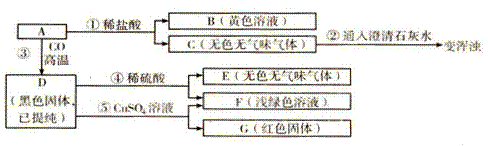 被誉为“江南小三峡”的南京胭脂河是明代初年开凿的一条人工运河,因其“石有胭脂色”而得名。胭脂河沿岸的那些红色石块的成分是什么?某研究性学习小组取一小块这种红色石块A,粉碎后对其成分进行实验探究,实验记录如下图所示:
被誉为“江南小三峡”的南京胭脂河是明代初年开凿的一条人工运河,因其“石有胭脂色”而得名。胭脂河沿岸的那些红色石块的成分是什么?某研究性学习小组取一小块这种红色石块A,粉碎后对其成分进行实验探究,实验记录如下图所示:
请根据实验推断:
A中含有的原子团是________(写离子符号)。B中肯定含有的溶质是_________(写化学式)。写出实验中有关反应的化学方程式:
②______________________________________; ⑤______________________________。
22. 实验室要测定某一氯化钠和碳酸钠混合物中氯化钠的质量分数,现有以下试剂和实验步骤可供选择,试剂:澄清石灰水、稀硫酸、氯化钡溶液。实验步骤:①称取少量混合物并溶解;②称量沉淀;③将产生的气体通人足量的某种试剂中;④向混合物中加入过量的某种试剂;⑤过滤沉淀并洗涤烘干;⑥实验数据计算。
请用两种方法测定混合物中氯化钠的质量分数,并在下表中写出每种测定方法中发生反应的化学方程式和测定的实验步骤的顺序(步骤用其序号表示,可重复选择)
|
方法 |
化学方程式 |
测定的实验步骤的顺序 |
|
(1) |
|
|
|
(2) |
|
|
22.有A、B、C、D四种无色溶液,分别是稀HCl、NaOH、MgSO4、NaCl溶液中的一种。某 同学只用紫色石蕊试液就将这四种溶液鉴别出来了。实验现象为:
①将紫色石蕊试液分别滴人装有A、B、C、D四种溶液的试管中,A变蓝,B不变,C、D变红;②另取A分别加入装有C、D溶液的试管中,C中无明显现象,D中有白色沉淀生成。
 根据上述实验可知,A中的溶质为___________;溶质为MgSO4的溶液是_____(填字母代号),该溶液呈_____性。
根据上述实验可知,A中的溶质为___________;溶质为MgSO4的溶液是_____(填字母代号),该溶液呈_____性。
24.有一包白色粉末可能由Na2SO4、Na2CO3、BaCl2、CuSO4中的一种或几种组成,小刚为了测定该白色粉末的组成,设计了如右图所示实验:
(1)白色沉淀A是__________;
(2)白色粉末中一定不含有___________,肯定含有_______________。
24.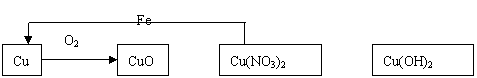 下图已标出四种含铜物质之间的部分转化关系。(1)请根据你对四种物质性质的理解,用“→”标出物质间其它的转化关系。要求“→”指向生成物,并且在“→”上标出参与反应物质的化学式。
下图已标出四种含铜物质之间的部分转化关系。(1)请根据你对四种物质性质的理解,用“→”标出物质间其它的转化关系。要求“→”指向生成物,并且在“→”上标出参与反应物质的化学式。
(2)写出上述转化关系中属于不同基本反应类型的两个化学方程式。
________________________________________, _______________________________________。
25.A、B、C、D、E为初中化学中的常见物质,并有如下转化关系:
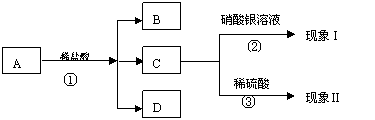
已知:A为白色固体,B为无色气体,E为现象Ⅰ中产生的不溶于稀硝酸的白色沉淀。
(1)写化学式:B____________ , E_____________;
(2)若现象Ⅱ为“产生白色沉淀”,则A可能为________________(写一种即可),有关反应的化学方程式为:①_____________________________;③___________________________。
若现象Ⅱ为“无明显现象”,则A可能为____________或_________________等。
26.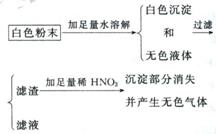 有一包白色粉末,可能含有CaCO3、BaCl2、Na2SO4、Na2CO3、K2SO4等物质,某同学对其进行了探究实验,实验过程如下:则该同学推测此白色粉末,至少由________种物质组成,其中一定含有的物质是________________。
有一包白色粉末,可能含有CaCO3、BaCl2、Na2SO4、Na2CO3、K2SO4等物质,某同学对其进行了探究实验,实验过程如下:则该同学推测此白色粉末,至少由________种物质组成,其中一定含有的物质是________________。
27.A、B、C、D是四种常见的物质,在自然界中能相互转化;A与B在一定条件下可以转化成C和D;C与D在一定条件下也可以转化成A和B。A在自然界中含量升高能引起温;室效应;C是一种糖类,在人体内经缓慢氧化提供能量。请你判断,A、B、C、D各是什么物质。A:____________ B:____________ C:__________ D:____________
28.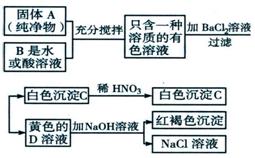 根据右图所示推断(假设能发生反应的均完全反应)
根据右图所示推断(假设能发生反应的均完全反应)
用化学式回答:
(1)D是_________________;
C是_________________。
(2)若B是水,则A是______________。
(3)若B是酸溶液,则A是__________或
___________。
(一)对废液作探究性假设
(1)若向废液中加入BaCl2溶液,产生白色沉淀,加足量稀硝酸沉淀不消失,则该白色沉淀可能是___________或_____________,不可能是________________。
(2)若向废液中加BaCl2溶液,产生白色沉淀,加足量稀硝酸沉淀会消失,并产生使澄清石灰水变得浑浊的气体,则原废液中一定含_______离子,一定不含______离子,也不含______离子(填符号,下同)
(3)若向废液中加BaCl2溶液,产生白色沉淀,加足量的稀硝酸沉淀部分消失,并产生使澄清石灰水变得浑浊的气体,则原溶液中一定含有_______离子和______离子。
1.现有甲、乙两种物质,已知其中一种是氧化镁,另外有A、B、C、D四种无色溶液,分别
是氢氧化钠溶液、硝酸镁溶液、硝酸钠溶液和稀硝酸中的一种,各物质间的转化关系如下列式子表示:
(1)乙+B →A+H2O (2)A+C→乙+D (3)甲+B→A+H2O
试判断:A是___________,C是________,乙是___________(用化学式回答)
2.现有A、B、C、D、E五种无色溶液,它们分别是硝酸银、盐酸、氯化钡、硫酸钠、碳酸钠中的一种。五种溶液之间反应现象如下(Ag2SO4视为可溶物)
|
实验 |
A+B |
A+C |
A+D |
C+D |
D+E |
A+E |
|
现象 |
有沉淀生成 |
有沉淀生成 |
有沉淀生成 |
有沉淀生成 |
有气体生成 |
无现象 |
根据以上实验现象可推断出:
A是________, B是__________,C是_________,D是______,E是__________。
3.有A、B、C、D、E、F六种化合物,其中A为金属氧化物,它们之间有下列转化关系(可溶物以溶液形式参加反应)
(1)A+B→C+D (2)C+NaOH→红褐色↓(E)+F (3)F+Ba(NO3)2→白色↓+NaNO3
写出下列物质的化学式:A_________B__________E___________F_____________
|
|
A |
B |
C |
D |
E |
|
A |
- |
↓ |
- |
- |
↓ |
|
B |
↓ |
- |
↑ |
- |
↓ |
|
C |
- |
↑ |
- |
- |
- |
|
D |
- |
- |
- |
- |
↓ |
|
E |
↓ |
↓ |
- |
↓ |
- |
4.有A、B、C、D、E五瓶失去标签的无色溶液,已知,它们分别是NaOH、HCl、BaCl2、MgSO4、K2CO3中的一种。为了鉴别,各取少量溶液两两混合,实验结果如图所示,其中“↓”表示生成难溶或微溶的沉淀, “↑”表示产生的气体,“-”表示观察不到现象(本实验条件下,微溶物以沉淀形式出现)
(1)根据实验现象,可判断A-E的物质名称是:
A________、B_______、C_______、D________、E________。
(2)请从A-E这5种物质中,选取适当物质,通过一种合理的途径制取氧化镁,按顺序写出各步反应的化学方程式。________________________________________________。
4.某工厂排放出一种澄清废液,一学校化学兴趣小组对该废液的成分进行如下探究分析:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com