
题目列表(包括答案和解析)
2、单质和化合物
|
|
单质 |
化合物 |
|
概念 |
由同一种元素组成的纯净物 |
由两种或两种以上的元素组成的纯净物 |
|
元素形态 |
元素处于游离态 |
元素处于化合态 |
|
性质 |
不能发生分解反应和复分解反应 |
大部分能发生分解反应和复分解反应 |
|
联系 |
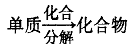 |
值得注意的是:①组成单质的虽是同一种元素,但在单质分子中,有单原子分子(一个原子构成一个分子),如稀有气体;有双原子分子(两个原子构成一个分子),如氢气、氧气;有多原子分子,如白磷,臭氧(O4),巴基球(C60)等。
②同种元素可以形成不同种单质,如白磷和红磷、氧气和臭氧,它们互为同素异形体。同素异形体在一定条件下能互相转化,这种转化是化学变化,如石墨转化为金刚石。

 混合物
混合物
 金属
金属
分类
单质
非金属
稀有气体
 纯净物
氧化物
纯净物
氧化物
酸
 无机化合物 碱
无机化合物 碱
化合物
盐 
有机化合物
1、纯净物和混合物
区别纯净物和混合物的关键点:是否由同一单质或化合物组成。
混合物的特点:①混合物是多种物质组成,各成分均是纯净物,这些纯净物彼此不发生化学反应,仍能保持各自的化学性质;②混合物无固定的组成,纯净物构成混合物时没有一定的比例,所以通常不以其中某一成分名称命名,而且混合物的物理性质也不同定;③从微观角度看,混合物是由多种彼此间不反应的分子、原子或离子构成,而纯净物是由同种分子、原子或离子构成。
3、(2008·苏州)由种类相同的元素组成的一组物质是( )
A、冰和干冰 B、银和水银 C、烧碱和纯碱 D、水和双氧水
2、(2009·南京)根据下表中相关信息,判断出的元素名称不一定合理的


1、(2009·东营)运用2008年诺贝尔化学奖的研究成果,可依据生物发光现象检测超微量钙的存在。这里的“钙”是指( )
A.分子
B.原子
C.元素 D.单质
4、元素与原子的比较
|
|
元素 |
原子 |
|
区别 |
是宏观概念,只表示种类不表示个数 |
是微观概念,既分种类,又表示个数 |
适用 范围 |
表示物质的宏观组成。 常用来表示物质由哪几种元素组成 |
表示物质的微观构成。 常用来表示物质的分子由哪些及几个原子构成 |
|
联系 |
只要核电荷数相同的一类原子就是同一种元素,原子是元素的最小单位,而元素是原子的一个归类“集体”。 |
[例2](2009·福州)海水是重要的资源,每千克海水中约含有钠10.62 g、镁1.28 g、钙0.40 g等。这里的“钠、镁、钙”指的是( )
A.原子
B.分子
C.元素 D.单质
[答案]C
[解析]此题是元素概念在实际生活中的应用。生活中的物质成分比较复杂,我们通常所说的物质组成都是指物质的元素组成,是通过元素组成来说明其成分或比较其含量的。
[规律小结]物质是由分子、原子或离子构成,由元素组成。
变式训练二
3、理解元素概念时的注意事项
(1)元素是以核电荷数(即质子数)为标准对原子分类。只论种类,不讲个数。
(2)质子数是划分元素种类的标准。质子数相同的原子和单核离子都属同一种元素。如Na+与Na都属钠元素,但Na+与NH4+不属于同一种元素。
(3)同种元素可以有不同的存在状态。如单质中和化合物中。
(4)同种元素的离子因带电荷数不同,性质也不同。如Fe2+与Fe3+。
(5)自然界中目前已知的元素有112种,可分为金属元素、非金属元素、稀有气体元素。
2、理解元素的概念应把握“同质子,类原子”六个字。
(1)“同质子”即指元素的种类是由核电荷数(即核内质子数)决定的,与原子中的中子数、电子数无关。同种元素原子的质子数一定相同,不同种元素的原子的质子数一定不相同。
(2)“类原子”是指一种元素可能不止一种原子。它包括质子数相同、中子数不同的原子(如:氢元素有三种原子:氕、氘、氚,它们的质子数相同,但中子数不同);也包括质子数相同,而电子数不同的原子和离子(如:铁原子通常有三种存在形式即Fe、Fe2+、Fe3+,它们都属于铁元素)。
1、元素的概念
元素是指具有相同核电荷数(即质子数)的同一类原子的总称。例如:氯
O +1 +3
+5 +7
元素包括C1-、Cl、Cl、C1、Cl、Cl…不同形式的粒子和Cl一35、Cl一37(指相对原子质量分别为35和37的两种氯原子)等粒子,因为它们的核电荷数均为17。
3、(2009·潍坊)下表呈现的是部分元素的原子结构示意图、主要化合价等信息。
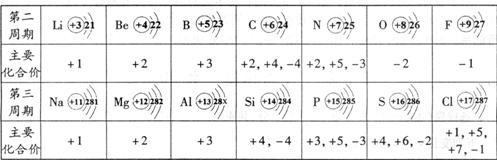

下列叙述错误的是( )
A.铝原子结构示意图的最外层有3个电子
B.元素的正化合价数一定等于原子的最外层电子数
C.核电荷数分别为8和14的元素,组成化合物的化学式为SiO2
D.同一周期中,原子的核外电子层数相同,最外层电子数从左向右逐渐增多
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com