
题目列表(包括答案和解析)
31.(2分)分子数相等的甲烷CH4与乙醇C2H5OH在氧气充足的条件下分别充分燃烧,生成水的质量较大的是 ;质量相等的甲烷CH4与乙醇C2H5OH在氧气充足的条件下分别充分燃烧。产生温室气体CO2质量较大的是 。
30.(2分)有一不纯的硫酸铵样品(样品中的杂质不含氮元素),经实验分析知道样品中氮元素的质量分数为20%,则样品里(NH4)2SO4的质量分数为 。(精确到0.1%)
29.(9分)某同学利用氢气还原灼热氧化铜的实验测定水的组成(装置如下图)。
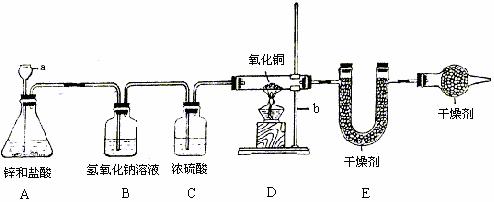
试回答下列有关问题:
(1)仪器a、b的名称为a ,b 。
(2)A中可观察到的现象为 ,D中可观察到的现象为
。
(3)B装置的作用是 ,C装置的作用是 。
(4)测定结果如下:实验前后D装置中玻璃管及其固体物质的质量分别为65.6g和59.2g,而实验前后E装置中U型管及其盛放物质的质量分别为100.8g和108.0g。则该同学测定的水中氢跟氧的质量比为 (必须列出算式并得出结果)。
(5)F装置的作用是吸收空气中的水蒸气,如不加F装置,实验结果将会比上述(4)中的测定结果 (选填“偏低”或“偏高”)。
28.(9分)某Na2CO3样品中混有少量NaCl,为测定该Na2CO3样品中Na2CO3的质量分数,某同学设计了一套实验装置(如下图所示)。
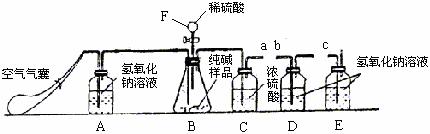
[实验原理]
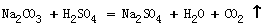
通过实验测定反应产生的CO2的质量,即可求得原样品中Na2CO3的质量,进而求得Na2CO3在样品中的质量分数。
[实验步骤]
① 如图连接装置(管口a、b、c暂不连接),并加入所需药品。
② 称量并记录装置D的质量(m1)。(称量时注意封闭此装置)
③ 挤压空气气囊,持续约1分钟。
④ 连接管口a、b、c。
⑤ 打开分液漏斗F的活塞,将稀硫酸快速加入B中后,关闭活塞。
⑥ 挤压空气气囊,持续约1分钟。
⑦ 称量并记录装置D的质量(m2)。(称量时注意封闭此装置)
⑧ 计算。
请填空回答下列问题:
(1)装置A的作用是 ;装置C的作用是 ;装置E的作用是
。步骤③操作的作用是 ;步骤⑥操作的作用是
(2)若所取Na2CO3样品的质量为5.3g,为确保实验顺利完成,分液漏斗F中至少要盛放10%的稀硫酸(密度为1.07g/mL) mL(精确到0.1)。若m1为51.20g,m2为53.18g,则样品中Na2CO3的质量分数为 。
27.(6分)一瓶无色溶液中可能含有NaCl、Na2CO3、Na2SO4、H2SO4、Ba(NO3)2中的一种或几种,某学生为了确定溶液中溶质的成分,做了如下实验:
(1)取少量溶液置于试管中,向其中滴加足量的BaCl2溶液,有白色沉淀产生。过滤后向沉淀中加入过量的稀硝酸,有一部分沉淀溶解,并有气泡产生。
(2)向上述实验所得的滤液中滴加AgNO3溶液,有白色沉淀产生,再加入足量的稀硝酸,沉淀不消失。
通过以上实验可知:该溶液中一定不含 ,原因是 。欲确定溶液中溶质的成分,应将该学生实验所用药品中的 调换成 。
26.(2分)要鉴别Na2CO3、NaOH、Ba(NO3)2三种无色溶液,可分别滴进一种试液,该试剂可以是 (写化学式);要鉴别KCl、KOH、BaCl2三种无色溶液,可分别滴进一种试液,该试剂可以是 (写化学式)。
25.(2分)要分离NaCl和BaCl2的混合溶液,可先向该溶液中加入稍过量的
溶液,过滤后,再分别向滤液和沉淀中加入适量的
24.(3分)某混合物气体由H2、N2、CO、CO2和HCl中的几种组成,现将其依次通过澄清石灰水(现象:无沉淀)、澄清石灰水(现象:有白色沉淀)、浓硫酸、灼热氧化铜(现象:黑色粉末变红)、无水硫酸铜(现象:白色粉末变蓝),据此可推知,该混合气体中一定含有 。(假设各装置中的反应或吸收都是完全的)
23.(2分)向盛有Mg、CuO和NaOH的固体混合物的烧杯中,加入一定量的稀硫酸,充分反应后过滤,再向滤液中滴入几滴酚酞试液,酚酞试液变成红色,则滤液中含有的溶质的化学式为 。
22.(2分)当氧气不充足时,乙醇(C2H5OH)燃烧生成CO、CO2和H2O。若乙醇燃烧产物中CO和CO2的总质量为12.8g,其中碳元素和氧元素的质量比为3:5,则参加反应的乙醇的质量为 g,产物中H2O的质量为 g。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com