
题目列表(包括答案和解析)
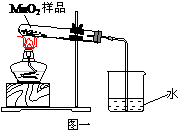
54. 兴趣小组在加热某二氧化锰样品时,意外地发现有气泡产生(如图一所示),于是他们对这个异常现象进行了研究。
① 对气体成分的研究。加热二氧化锰用带火星的木条靠近试管口,木条熄灭。将气体通入澄清的石灰水,发现石灰水变浑浊。产生的气体是(13)。
② 对气体的来源的研究。
[假设1]甲同学认为该气体来自于试管中的空气,请你设计实验证明该假设不成立
|
实验步骤及现象 |
结论 |
|
(14) |
假设不成立。 |
[假设2]乙同学认为:二氧化锰中可能混有碳粉,碳粉发生反应生成了该气体。他设计了如图二所示的实验进行研究。其中B装置的作用是检验A中反应是否完全,B中溶液的溶质是 (15) 。实验中观察到D处澄清石灰水变浑浊。他又用氮气代替空气(氮气不参与该实验中的任何反应),发现D处澄清的石灰水也变浑浊。
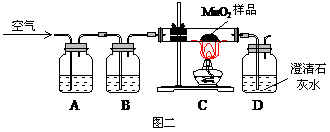
[结论]二氧化锰中混有碳粉,碳粉与 (16) 反应产生了这种气体。
53. 如图所示,实验室有一瓶标签被部分腐蚀的盐溶液,为确定其成分几位同学进行了如下研究。
|
[提出假设]几位同学对其溶质提出了不同的假设 甲同学认为:可能是NaCl 乙同学认为:可能是NaOH 丙同学认为:可能是Na2CO3 丁同学认为:可能是Na2SO4 |
 |
上述假设中一定错误的是(7),除上述假设外你认为该溶液还有可能是 (8)溶液。
[实验探究]排除了错误的假设后,几位同学设计了如下方案,通过实验,验证他们的假设,请完成实验报告
|
实验步骤 |
现象 |
结论 |
|
|
Ⅰ |
取样于试管中,向其中滴加
(9) |
(10) |
待测液不是Na2CO3溶液 |
|
Ⅱ |
向实验Ⅰ的试管中滴加Ba(NO3)2溶液 |
无明显现象 |
待测液不是(11) 溶液 |
|
Ⅲ |
向实验Ⅱ的试管中滴加
(12) |
产生白色沉淀 |
待测液是NaCl溶液 |
52. 实验室有一瓶500 mL含有硫酸的废液,恰好中和这些硫酸消耗氢氧化钠0.1mol 。
① 废液中含H2SO4的物质的量是多少?(根据化学方程式列式计算)
② 若废液的密度是1.0g/ mL,则废液中硫酸的质量分数是 (6) 。
请根据要求在答题纸相应的位置作答。
51. 某班同学在实验室进行制取二氧化碳气体的实验。可供选择的实验装置如下
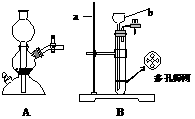
① 仪器a和b的名称:a (1) ,b (2) 。
② 用启普发生器制取二氧化碳气体,反应的化学方程式是 (3) 。
③ B装置具有启普发生器随开随用、随关随停的优点,本实验中多孔筛网的材料一定不能是(4) ,理由是 (5) 。
A、塑料 B、玻璃 C、铁 D、铜
50. 某工厂排出的废液中主要含有硝酸锌和硝酸银。为回收金属银和硝酸锌,某同学设计了如下实验。其中固体A是(16) ,滤液C的溶质是(17) ,操作M是(18) ,

49. 如图是A、B两种固体的溶解度曲线,请回答下列问题
|
① 10℃时,S(A) (12) S(B)。 (填“>”、“<”或“=”) ② 30℃时,B的溶解度为 (13) g/100g水; ③ A中混有少量B,提纯A可采用的方法是 (14) 。 ④ 50℃时,恰好完全溶解120 g A形成饱和溶液,需要水 (15) g |
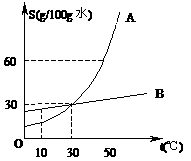 |
48. 由钛铁矿(主要成分是FeO和TiO2)提取金属钛的主要工艺流程如下。
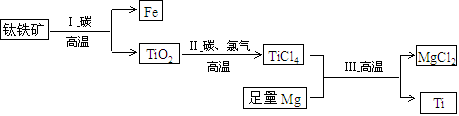
① 上述流程中的物质属于氧化物的是 (6) ,属于金属单质的是 (7) ,TiO2中钛元素的化合价是 (8) 。
② 步骤Ⅰ中,FeO和碳反应生成二氧化碳和铁,化学方程式是 (9) ,该反应中还原剂是 (10)
③ 步骤Ⅲ的基本反应类型是 (11) 。
请将结果填入答题纸的相应位置。
47. 通过化学学习我们认识了很多身边的物质,请回答
① 氮气约占空气体积的 (1) ;
② 可以做干电池电极的是 (2) (填名称);
③ 温度计中的液态金属是 (3) ;(填化学式)
④ 与人体血液中血红蛋白结合使人中毒的气体是(4)
⑤ 碳酸钙是很多补钙药品的主要成分,碳酸钙中钙元素的质量分数是 (5) 。
46. 如图所示,用氢气还原w mol氧化铜,实验中当看到大部分黑色固体变成光亮的红色时,停止加热。共消耗x mol氢气,生成y mol水和z mol铜。下列说法正确的是
|
A、反应后玻璃管内固体质量为64z g B、反应前后玻璃管内固体的质量之差是16w g C、玻璃管中固体减少的质量就是N装置中固体 增加的质量 D、z=y<x |
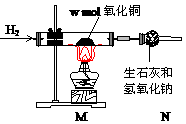 |
45. “物质的量”是国际单位制中的一个基本物理量,有关说法正确的是
A、18 g H2O中含有1mol氢 B、1 mol小钢珠中约有6.02×1023个钢珠
C、C60的摩尔质量为720 D、1 mol O3中约含有1.806×1024个氧原子
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com