
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
22Ўў(ёч1·ЦЈ¬№І2·Ц)
ЎЎЎЎЎЎЎЎ (1)nN2ЎЎЎЎЎЎ (2)5Na+
ЎЎ ЖА·ЦЛөГч:»ҜС§·ҪіМКҪЖА·Ц·Ҫ·Ё(Въ·ЦОӘ2·Ц)Ј¬»ҜС§КҪҙнІ»ёш·ЦЈ¬ЕдЖҪҙнҝЫ1·ЦЈ¬Мхјю»тјэН·ҙнұҫРЎМв№ІҝЫl·ЦЎЈ
21Ўў(2·Ц)48
31.(6·Ц)ТСЦӘCuSO4ИЬТәПФА¶Й«Ј¬ёГИЬТәЦРә¬УРҪП¶аөДCu2+әНSO42-АлЧУ ЎЈ
(1)МбіцОКМв:ИЬТәөДСХЙ«КЗУЙКІГҙАлЧУТэЖрөДЎЈ
ЎЎЎЎ ПЦУРКФјБ:K 2SO4ИЬТә ЎўNaOHИЬТәЎўBaCl2ИЬТәЎўРҝ·ЫЈ¬
ЎЎЎЎ ПЦУРТЗЖч:КФ№ЬЎўЙХұӯЎўМъјЬМЁ(ҙшМъИҰ)ЎўВ©¶·ЎўВЛЦҪЎўІЈБ§°ф
(2)јЩЙи:ИЬТәөДА¶Й«КЗУЙТэЖрөДCu2+ -Ј¬¶шІ»КЗУЙSO42ТэЖрөДЈ¬
(3)СйЦӨ:
|
ІЩЧчІҪЦи |
ПЦПуәНҪбВЫ |
|
ЎЎ ЎЎ ЎЎ |
ЎЎ |
ҙр°ёј°ЖА·ЦТвјы
30.(8·Ц)НЁ№э»ҜС§КөСйјшұрОпЦКөДҙжФЪЈ¬ПЦПу·ЦОцәННЖАн№эіМКЗК®·ЦЦШТӘөДЎЈПЦУР№ММе»мәПОпТ»°ьЈ¬ҝЙДЬУЙKNO3ЎўNaClЎўK2SO4ЎўBaSO4ЎўCaCl2ЎўNa2CO3ЦРөДТ»ЦЦ»тјёЦЦЧйіЙЈ¬ТАҙОҪшРРКөСйЈ¬ЗлНкіЙИзПВКөСйјЗВј·ЦОцұЁёжЎЈ
|
КөСйІҪЦи |
№ЫІмПЦПу |
¶ФУҰөДНЖАнәН·ЦОц |
|
1Пт»мәПОпЦРјУИлККБҝЛ® |
И«ІҝИЬҪвЈ¬ИЬТәОЮЙ«НёГч |
1Т»¶ЁГ»УР: |
|
2ПтІҪЦи1ИЬТәЦРөОјУ №эБҝBaC l2ИЬТә |
°ЧЙ«іБөн ЎЎ |
2ҝЙДЬУР: |
|
3ИЎІҪЦи2өД°ЧЙ«іБөнЈ¬ јУИлПЎСОЛб |
°ЧЙ«іБөнИ«ІҝПыК§ ЎЎ |
3Т»¶ЁУР: |
|
4ФЪІҪЦи2өДЧЗТәЦРөОјУ №эБҝAgNO3ИЬТәәНПЎHNO3 |
°ЧЙ«іБөн ЎЎ |
4Т»¶ЁУРNaClәНCaCl2 |
ОК:(1) ІҪЦи4НЖАн·ЦОцКЗ·сХэИ·Ј¬Из№ыІ»ХэИ·, ЛөГчФӯТт, Из№ыХэИ·І»УГВЫКц:ЎЎЎЎЎЎЎЎ
ЎЎ (2)№ММе»мәПОпІ»Т»¶Ёә¬УРЎЎЎЎЎЎЎЎЎЎЎЎ
29.(6·Ц)°ҙПВНјЧ°ЦГҪшРРКөСйЈ¬ІЈБ§№ЬAЦРөДәЪЙ«·ЫД©ҝЙДЬКЗҙҝҫ»Оп»т»мәПОпЎЈ
ЎЎ 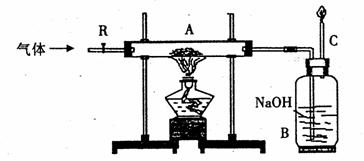
(1)ҙтҝӘ»оИыRЈ¬ИфНЁИЛCO2ЖшМеЈ¬CҙҰУРҝЙИјРФЖшМеИјЙХЈ¬ФтAҙҰәЪЙ«·ЫД©КЗЎЎЎЎЎЎЎЎЎЎ
AҙҰ·ҙУҰөД»ҜС§·ҪіМКҪОӘ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎCҙҰөДЧчУГКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
(2)Иф№ШұХ»оИыR, јУИИәуAҙҰәЪЙ«·ЫД©ұдОӘәмЙ«, ФтAҙҰәЪЙ«·ЫД©КЗЎЎЎЎЎЎЎЎЎЎ , BЎўCҙҰГ»УРГчПФПЦПуЎЈИфТӘЦӨГчBЦРИ·Кө·ўЙъБЛ»ҜС§·ҙУҰЈ¬ЙъіЙРВөДОпЦКЈ¬КөСй·Ҫ·ЁәН№ЫІмөҪөДПЦПуКЗ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈ
28Ј®(6·Ц)КөСйКТМṩИзПВНјЛщКҫөДТЗЖчЈә
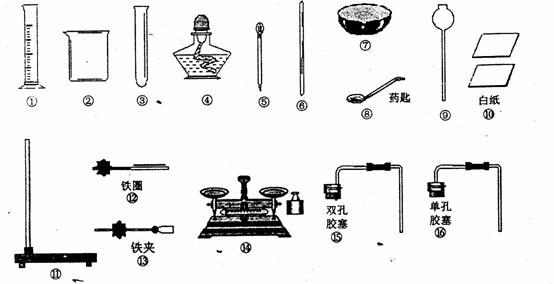
(1)ЦёіцПВБРТЗЖчГыіЖ:
ЎЎўЫЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎ;ЎЎ ўЬ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ; ўЭЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
(2)НкіЙПВБР»ҜС§КөСйЈ¬РиТӘөДТЗЖчКЗ(УГұаәЕ»Шҙр):
ЎЎ1іЖБҝ15gөДКіСО№ММеЈ¬РиТӘөДТЗЖчКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
ЎЎ2Хф·ўұҘәНКіСОИЬТәөД№эіМЦРЈ¬К№УГЎЎЎЎЎЎ ТЗЖчҝЙ·АЦ№ИЬТә·ЙҪҰіцАҙЎЈ
ЎЎ3КөСйКТЦЖ¶юСх»ҜМјЈ¬РиТӘөДТЗЖчіэ3111315УГНвЈ¬»№РиТӘөДТЗЖчКЗЎЎЎЎЎЎЎЎЎЎ
27Ј®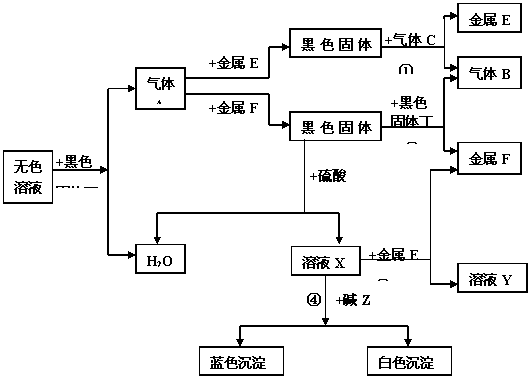 (9·Ц)ПВНјКЗіЈјыОпЦКјдПа»ҘЧӘ»ҜөД№ШПөНјЎЈТСЦӘҪрКфFЎўEөДПа¶ФФӯЧУЦКБҝЦ®ІоОӘ8Ј¬ЖдЛы·ҙУҰМхјюТСКЎВФЎЈ
(9·Ц)ПВНјКЗіЈјыОпЦКјдПа»ҘЧӘ»ҜөД№ШПөНјЎЈТСЦӘҪрКфFЎўEөДПа¶ФФӯЧУЦКБҝЦ®ІоОӘ8Ј¬ЖдЛы·ҙУҰМхјюТСКЎВФЎЈ
ҫЭЙПНј№ШПө»Шҙр:
(1)ЖшМеAөД»ҜС§КҪОӘЎЎЎЎЎЎЎЎЎЎЎЎЎЎ әЪЙ«№ММеұыөД»ҜС§КҪЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
(2)·ҙУҰ2өД»щұҫ·ҙУҰАаРНКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ·ҙУҰ
(3)Рҙіц·ҙУҰ134өД»ҜС§·ҪіМКҪ:
1ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
3ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
4ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
26Ј®(6·Ц)¶юСх»ҜМјЖшМеКЗОТГЗФЪЙъ»оЦРіЈјыөДЖшМеЈ¬Зл°ҙМвДҝөДТӘЗуРҙіцУР¶юСх»ҜМјІОјУ»тЙъіЙөД»ҜС§·ҙУҰ·ҪіМКҪЎЈ
ЎЎЎЎ (1)УЙSO2өИЖшМеРОіЙөДЛбУк(H2SO4)ёҜКҙМм°ІГЕЗ°өД»Әұн:ЎЎЎЎЎЎЎЎ ЎЎЎЎЎЎЎЎ
ЎЎЎЎ (2)УГКҜ»ТЛ®Лў№эөДЗҪұЪ№эТ»¶ОКұјдұд°ЧұдУІ:ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
ЎЎЎЎ (3)јЧНйИјЙХІъЙъИИБҝ:ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
25Ј®(2·Ц)УГІв¶Ё1m3ұ»ёЙФпөДҝХЖшЦРЙРКЈУаөДЛ®ХфЖыә¬Бҝ(g)өД¶аЙЩАҙұИҪПёчЦЦёЙФпјБөДёЙФпР§ВКЎЈЛ®ХфЖыә¬БҝФҪЙЩЈ¬ёЙФпјБөДёЙФпР§ВКФҪёЯЎЈПВұнБРіціЈУГёЙФпјБөДёЙФпР§ВК:
|
ёЙФпјБ |
CuSO4 |
NaOH |
KOH |
ЕЁH2SO4 |
|
Л®ХфЖыә¬Бҝ(g/m3) |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЗлОКЈ¬ёЙФпCO2ЧоәГСЎУГЎЎЎЎЎЎЎЎЎЎ ёЙФпјБЈ¬ёЙФпO2ЧоәГСЎУГЎЎЎЎЎЎЎЎЎЎ ФпјБЎЈ
24Ј®(8·Ц)№ӨТөЙПОӘБЛІв¶ЁБтЛбөДЕЁ¶И(ИЬЦКөДЦКБҝ·ЦКэ)Ј¬іЈУГТ»¶ЁұкЧјЕЁ¶ИөДЗвСх»ҜДЖИЬТәУлБтЛб·ҙУҰЈ¬»ҜС§·ҙУҰ·ҪіМКҪКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЎЈ
(1)КЧПИЈ¬ЕдЦЖЦКБҝ·ЦКэОӘ10%өДЗвСх»ҜДЖИЬТә120gЈ¬РиТӘЎЎЎЎ gЗвСх»ҜДЖ№ММеәНЛ®ЎЎЎЎ g
(2)ЕдЦЖЦКБҝ·ЦКэОӘ10%өДЗвСх»ҜДЖИЬТәІЩЧчІҪЦијыПВНјЈ¬ХэИ·өДІЩЧчЛіРтКЗЎЎЎЎЎЎЎЎЎЎ
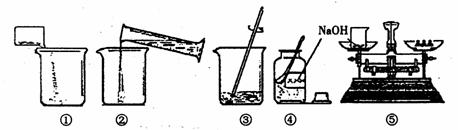
(3)УГЙПКцЕдәГөД10%ЗвСх»ҜДЖИЬТә40gУлБтЛб·ҙУҰЈ¬ТФ·УМӘЧчЦёКҫјБЈ¬өұҝҙөҪ»мәПИЬТәөДСХЙ«УЙәмЙ«ёХәГұдОӘОЮЙ«КұЈ¬јЗВј·ҙУҰЦРәДУГБтЛбИЬТәЦКБҝОӘ98gЈ¬ФтёГБтЛбөДИЬЦКЦКБҝ·ЦКэКЗЎЎЎЎЎЎ
№ъјКѧУУЕСЎ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com