
题目列表(包括答案和解析)
3. 下列物质中,导电性能最差的是( )
A. 石墨棒 B. 盐酸溶液 C. 熔融的氢氧化钠 D. 固体氯化钾
2. 下面关于电解质电离的叙述正确的是( )
A. CaCO3在水中溶解度很小,其导电能力很弱,所以 CaCO3是弱电解质
B. CaCO3在水中溶解度很小,但溶解的 CaCO3全部电离,所以 CaCO3是强电解质
 C. 氯气和氨气的水溶液导电性都很好,所以它们是强电解质
C. 氯气和氨气的水溶液导电性都很好,所以它们是强电解质
D. 水难电离,纯水几乎不导电,水是非电解质
1. 下列状态的物质,既能导电又属于电解质的是( )
A. MgCl2 晶体 B. NaCl 溶液 C. 液态氯化氢 D. 熔融的KOH
可能用到的相对原子质量:Cu-64
24. 1.28 g 的铜与足量的浓硝酸充分反应后,可收集到气体多少mL(标况下)?被还原的硝酸的物质的量是多少?

23. 现欲设计一个实验,验证红热的炭与浓硫酸发生反应所生成的各种产物。有一个同学按气体的流动方向设计了一个实验流程,其所使用的试剂次序可表示为:气体产物→无水硫酸铜→品红溶液→溴水→品红溶液→澄清石灰水

(1)①中反应的化学方程式为 ;
(2)②处的现象是: 。
(3)品红溶液使用了两次,第一次使用时的作用是
第二次使用时的作用是________________ _。
(4)④的作用是: 。
(5)二氧化硫也能使溴水褪色,表现了二氧化硫的 性。(“还原”、“漂白”)
反应的化学方程式为: 。
(6)根据 现象,可证明产物中一定有CO2气体
22. 某非金属单质A经如下图所示的过程转化为含氧酸D,已知D为强酸,请回答下列问题:

(1)若A常温下为淡黄色固体,B是有刺激性气味的无色气体。
①A的化学式:
②工业生产中大量排放的B气体被雨水吸收后形成 而污染环境。
③写出B→C反应的化学方程式:
(2)若A在常温下为气体,C是红棕色气体。
①A、C的化学式分别是:A ,C
②写出B→C反应的化学方程式:
 ③D的浓溶液在常温下可与木炭反应并生成C气体,该反应的化学方程式为:
③D的浓溶液在常温下可与木炭反应并生成C气体,该反应的化学方程式为:
。
21. 硝酸工厂的尾气氮氧化合物若不加以处理排放到大气中,不仅会形成硝酸型酸雨,还可以形成光化学烟雾。因此必须对含有氮氧化合物的废气进行处理。
(1)用氢氧化钠溶液可以吸收废气中的氮氧化合物,反应的化学方程式为:
NO2 + NO + 2NaOH == 2NaNO2 + H2O
标出电子转移的方向和数目。在该反应中,每生成1 mol NaNO2、转移电子的数目为 。
(2)汽车尾气中含有NO和CO,消除这两种物质对大气污染的方法是安装催化转化器,使它们发生反应生成N2和CO2。该反应的化学方程式为:
。
氧化剂是 ,还原剂是 。
20. 

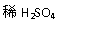 用铜和浓硫酸为原料制取硫酸铜时,可用下列两种方案:
用铜和浓硫酸为原料制取硫酸铜时,可用下列两种方案:
甲方案:Cu---→CuSO4 乙方案:Cu--→CuO---→CuSO4
写出甲方案的化学方程式:
这两种方案对比, 方案更好,理由是:
19. 请写出反应的化学方程式:
(1)用NaOH溶液吸收SO2气体:
(2)工业上采用接触法制硫酸,其中在接触室进行的反应是:
(3)铜与稀硝酸反应:
18.  利用氧化还原反应原理配平
利用氧化还原反应原理配平
NH3
+ O2  NO + H2O
NO + H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com