
题目列表(包括答案和解析)
14、某原电池总反应的离子方程式为:2Fe3++Fe=3Fe2+,能实现该反应的电池是
A.正极为Cu,负极为Fe,电解质为FeCl2溶液
B.正极为Cu,负极为Fe,电解质为Fe(NO3)3溶液
C.正极为Cu,负极为Zn,电解质为Fe2(SO4)3溶液
D.正极为Ag,负极为Fe,电解质为CuSO4溶液
13、下列化学反应既属于化合反应又属于吸热反应的是
A.铝片和稀盐酸反应 B.氢氧化钡晶体和氯化铵反应
C.灼热的碳与CO2反应 D.碳酸钙高温分解
12、在一定温度下,反应A2(气)+ B2(气) 2AB(气)达到平衡的标志是
2AB(气)达到平衡的标志是
A.单位时间生成的n mol的A2同时生成n mol的AB
B.容器内的总压强不随时间变化
C.单位时间生成2n mol的AB同时生成n mol的B2
D.单位时间生成n mol的A2同时生成n mol的B2
11、对于锌一铜一稀硫酸组成的原电池装置中,当导线中有1 mol电子通过时,理论上的两极变化是( )。
①锌片溶解了32.5g ②锌片增重32.5g
③铜片上析出lg H2 ④铜片上析出1mol H2
A.①和③ B.①和④ C.②和③ D.②和④
10、镍镉(Ni-Cd)可充电电池在现代生活中有广泛的应用,它的充电放电反应按下式进行: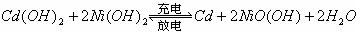
由此可知,该电池放电时的负极材料是( )
A.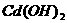 B.
B.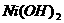
C.Cd D.
9、控制适合的条件,将反应2Fe3++2I- 2Fe2++I2设计成如右图所示的原电池(盐桥起到导电作用)。下列判断不正确的是
2Fe2++I2设计成如右图所示的原电池(盐桥起到导电作用)。下列判断不正确的是
A.反应开始时,乙中石墨电极上发生氧化反应
B.反应开始时,甲中石墨电极作负极
C.电流计读数为零时,反应达到化学平衡状态
D.电流计读数为零后,在甲中溶入FeCl2,电流表可能会再次产生偏转。
8、 A、B、C、D四种短周期元素的原子半径依次减小,A与C的核电荷数之比为3:4,D能分别与A、B、C形成电子总数相等的分子X、Y、Z。下列叙述正确的是
A.X、Y、Z的稳定性逐渐减弱
B.A、B、C、D只能形成5种单质
C.X、Y、Z三种化合物的熔沸点逐渐降低
D.自然界存在多种由A、B、C、D四种元素组成的化合物
7、已知短周期元素的离子:aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是
A.原子半径 A>B>D>C B.原子序数 d>c>b>a
C.离子半径 C>D>B>A D.单质的还原性 A>B>D>C
6、下列各组物质中,分子中的所有原子都满足最外层8电子结构的是
A.BeCl2、PCl5 B.PCl3、N2
C.COCl2(光气)、SF6 D.XeF2、BF3。
5、下列离子方程式书写正确的是( )。
A.烧碱溶液与小苏打溶液反应:OH-+HCO3- H2O+CO2↑
B.铝粉与烧碱溶液反应:2Al+2OH-+2H2O 2AlO2-+3H2↑
C.氯化亚铁溶液中滴加氯水: Fe2++Cl2 Fe3++2Cl-
D.氯气通入冷的氢氧化钠溶液中:2Cl2
+ 2OH- 3Cl- + ClO- +
H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com