
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
4£Æ¿’…≥Ãÿ¡–‘≠¿Ì «◊‘»ªΩÁ“ªÃı÷ÿ“™µƒª˘±æ‘≠¿Ì£¨ ‘‘À”√¥À‘≠¿Ì∑÷Œˆ£∫¬»ªØ“¯‘⁄œ¬¡–»Ð“∫÷–»ÐΩ‚∂»◊Ó…Ÿµƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°
°°°° A. ±•∫Õ ≥—ŒÀÆ°°°°°°°°°°°°°°°°°°°°°° B. 0.1 mol£ØLµƒ—ŒÀ·
°°°° C. 0.1 mol£ØLµƒCaCl2»Ð“∫°°°°°°°°°° D. –¬÷∆µƒ±•∫Õ¬»ÀÆ
3£ÆœÚ4 L»ð∆˜÷–≥‰»Î0.7 mol SO2∫Õ0.4 mol O2£¨4 sƒ©≤‚µ√ £”ýSO2 «0.3 mol£¨‘Úu(O2)Œ™°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °°°°°°°°°°°°°°
°°°°°° A. 0.100 mol /(L°§min)°°°°°°°°°°°°°° B. 0.025 mol /(L°§s)
°°°°°° D. 0.050 mol /(L°§min)°°°° °°°°°°°°°°D. 0.0125 mol /(L°§s)
2£Æ‘⁄µ»Œ¬°¢µ»»ðÃıº˛œ¬”–œ¬¡–∆¯ÃÂ∑¥”¶£∫2A(∆¯)+2B(∆¯) C(∆¯)+3D(∆¯)°£œ÷∑÷±¥”¡ΩÕææ∂Ω®¡¢∆Ω∫‚£∫I A∫ÕBµƒ∆ º≈®∂»æ˘Œ™2mol/L£ªII C∫ÕDµƒ∆ º≈®∂»∑÷±Œ™2 mol/L∫Õ6mol/L°£œ¬¡–– ˆ’˝»∑µƒ «
C(∆¯)+3D(∆¯)°£œ÷∑÷±¥”¡ΩÕææ∂Ω®¡¢∆Ω∫‚£∫I A∫ÕBµƒ∆ º≈®∂»æ˘Œ™2mol/L£ªII C∫ÕDµƒ∆ º≈®∂»∑÷±Œ™2 mol/L∫Õ6mol/L°£œ¬¡–– ˆ’˝»∑µƒ «
A£ÆI∫ÕII¡ΩÕææ∂◊Ó÷’¥ÔµΩ∆Ω∫‚ ±£¨ÃÂœµƒ⁄ªÏ∫œ∆¯ÃµƒÃª˝∑÷ ˝œýÕ¨
B£ÆI∫ÕII¡ΩÕææ∂◊Ó÷’¥ÔµΩ∆Ω∫‚ ±£¨ÃÂœµƒ⁄ªÏ∫œ∆¯ÃµƒÃª˝∑÷ ˝≤ªÕ¨
C£Æ¥Ô∆Ω∫‚ ±£¨IÕææ∂µƒ∑¥”¶ÀŸ¬ µ»”⁄IIÕææ∂µƒ∑¥”¶ÀŸ¬
D£Æ¥Ô∆Ω∫‚ ±£¨IÕææ∂ªÏ∫œ∆¯ÃÂ√Ð∂»Œ™IIÕææ∂ªÏ∫œ∆¯ÃÂ√Ð∂»µƒ1/2
1£Æ“ª∂®Œ¬∂»œ¬£¨œÚ“ª»ðª˝Œ™2 Lµƒ’Êø’√б’»ð∆˜÷–( ¬œ»◊∞»Î¥þªØº¡)Õ®»Î1 mol µ™∆¯∫Õ3 mol«‚∆¯°£3 min∫Û≤‚µ√»ð∆˜ƒ⁄µ™∆¯µƒŒÔ÷ µƒ¡øŒ™0.8 mol°£‘⁄¥À ±º‰ƒ⁄£¨ ”√«‚∆¯µƒ¡øµƒ±‰ªØ¿¥±Ì æ∏√∑¥”¶µƒ∆Ωæ˘ÀŸ¬ 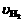 «°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
«°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
°°°° A. 0.6 mol£Ø(L°§min)°°°°°°°°°°°°°°°°°° B. 0.3 mol£Ø(L°§min)
°°°° C. 0.2 mol£Ø(L°§min)°°°°°°°°°°°°°°°°°° D. 0.1 mol£Ø(L°§min)
≤˙ŒÔ“ª£∫°° H2°° £¨”√Õæ£∫ ∫œ≥…∞±º∞∫œ≥…∆˚”Õµƒ‘≠¡œ°° £ª
≤˙ŒÔ“ª£∫°° C °°£¨”√Õæ£∫°° œΩ∫𧓵µƒ‘≠¡œ°°°° °£
2£Æ1moL CH4”ÎCl2‘⁄…’∆øƒ⁄∑¢…˙»°¥˙∑¥”¶£¨¥˝∑¥”¶ÕÍ»´∫Û£¨≤‚µ√Àƒ÷÷»°¥˙ŒÔµƒŒÔ÷ µƒ¡øœýµ»£¨‘Úœ˚∫ƒCl2Œ™( B°° )moL£ª…˙≥…HCl(°° B )moL£ª…˙≥…µƒ∆¯ÃÂ◊ÐŒÔ÷ µƒ¡øŒ™(°° C )moL
A.0.5°°°° B.2.5°°°° C.2.75°°°° D.4
1£Æπ‚’’Ãıº˛œ¬£¨Ω´µ»ŒÔ÷ µƒ¡øµƒCH4”ÎCl2ªÏ‘⁄ºØ∆¯∆ø÷–£¨æ≠π‚’’≥‰∑÷∑¥”¶∫Û£¨µ√µΩ≤˙ŒÔµƒŒÔ÷ µƒ¡ø◊Ó∂ýµƒ «( D°° )
A.CH3Cl°°°° B.CH2Cl2°°°° C.CHCl3°°°° D.HCl
¥À ±∆ø÷–π≤”–º∏÷÷ŒÔ÷ ( D°° )
A.Àƒ÷÷°° B.ŒÂ÷÷°° C.¡˘÷÷°° D.∆þ÷÷
5£ÆΩ´“ª∂®¡øµƒCH4°¢O2∫ÕNa2O2∑≈‘⁄“ª√б’»ð∆˜÷–£¨”√µÁªª®≤ª∂œ“˝»ºªÏ∫œ∆¯Ã£¨ π∆‰≥‰∑÷∑¥”¶°£Ω· ¯∫Û£¨»ð∆˜ƒ⁄µƒ—π«ø«˜”⁄¡„£¨∆‰ £”ýπÃûДÎÀÆŒÞ∆¯ÃÂ∑≈≥ˆ°£
¢≈”–πÿNa2O2∑¥”¶∑Ω≥Ã Ω°° 2CH4 + O2 + 6Na2O2 £Ω2Na2CO3 + 8NaOH°°°°°° °°°°
¢∆«ÛCH4°¢O2°¢Na2O2µƒŒÔ÷ µƒ¡ø÷Ʊ»Œ™°° 2:1:6°°°°°°°°°°
4.≥£Œ¬œ¬£¨º◊ÕÈ”Î◊„¡øµƒ—ı∆¯µƒªÏ∫œ∆¯ÃÂπ≤57mL£¨µ„»º±¨’®∫Û£¨ £”ý∆¯ÃÂŒ™23mL(ª÷∏¥µΩ‘≠◊¥Ã¨)°£«Û‘≠ªÏ∫œ∆¯ÃÂ÷–º◊ÕȵƒÃª˝°£17mL
3.“ª∂®÷ ¡øµƒº◊ÕÈ≤ªÕÍ»´»º…’µ√µΩµƒ≤˙ŒÔŒ™CO,CO2∫ÕÀÆ’Ù∆¯£¨¥À ±ªÏ∫œ∆¯ÃÂ÷ ¡øŒ™49.6g£¨µ±∆‰ª∫¬˝Õ®π˝ŒÞÀÆCaCl2 ±£¨CaCl2÷ ¡ø‘ˆº”25.2g°£‘≠ªÏ∫œ∆¯ÃÂ÷–CO2µƒ÷ ¡øŒ™°°°° (°° C°° )
A.24.4g°°°° B.19.7g°° C.13.2g°° D.12.5g
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com