
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
4.æ≠ø∆—ß—–æø∑¢œ÷£¨‘™Àÿ‘≠◊”◊ÓÕ‚≤„µÁ◊” ˝ «8ªÚµ⁄“ª≤„Œ™◊ÓÕ‚≤„«“µÁ◊” ˝Œ™2µƒ‘≠◊” «∫ÐŒ»∂®µƒ£¨∂¯◊ÓÕ‚µÁ◊”≤„µÁ◊” ˝ «1µƒ‘™Àÿ»ð“◊ ß»•’‚∏ˆµÁ◊”£¨◊ÓÕ‚≤„µÁ◊” ˝ «7µƒ‘≠◊”»ð“◊µ√µΩµÁ◊”£¨»Áπ˚‘≠◊”◊ÓÕ‚≤„µÁ◊” ˝ «4£¨∆‰µ•÷ ‘⁄µºµÁ∑Ω√Êæþ”–ƒ≥–©Ãÿ ‚µƒ”≈¡º–‘ƒÐ£¨»ÁπË‘≠◊”◊ÓÕ‚µÁ◊”≤„”–4∏ˆµÁ◊”£¨“Ú∂¯≥£±ª”√◊˜∞εºÃÂ≤ƒ¡œ°£œ¬¡–ø…◊˜∞εºÃÂ≤ƒ¡œµƒ «(°°°° )

Àº¬∑Ω‚Œˆ£∫∂‘±æ–≈œ¢µƒ¥¶¿Ì“™◊¢“‚»•Œ±¥Ê’Ê£¨≈≈≥˝∏…»≈°£Ã‚∏…÷–∏¯≥ˆ¡À∞εºÃÂ≤ƒ¡œ‘≠◊”Ω·ππµƒ√˜œ‘–≈œ¢£¨º¥‘≠◊”µƒ◊ÓÕ‚≤„µÁ◊” ˝ «4°£
¥∞∏£∫C
øÏ¿÷ ±π‚
∂¡–°—ßÀƒƒÍº∂µƒµÐµÐ≈÷µ√ µ‘⁄≤ªœÒª∞£¨¥Ûº“≥£≥£»°–¶À˚°£
“ªÃÏ£¨¿œ ¶“™À˚√«“ª∞ýÕ¨—ßø™ º‘⁄¡™¬Á≤æ…œº«œ¬°∞√øÃÏ∞Ôº“¿Ô◊ˆµƒ ¬°±£¨µÐµÐ‘ı√¥“≤œÎ≤ª≥ˆ¿¥£¨◊Ó∫Û÷ª∫√”…¬Ë¬Ë¥˙Œ™ÃÓ–¥°£À˝‘⁄¡™¬Á≤æ…œ–¥¡À£∫°∞√øÃÏ∞Ôº“¿Ô≥‘∑π°±°£¿œ ¶µƒ∆¿”Ô «£∫°∞ø¥µ√≥ˆ¿¥£¨ƒ„∫Ð≈¨¡¶£°°±
30 ∑÷÷”—µ¡∑(πÆπÿý—µ¡∑£¨ø…”√”⁄øŒ∫Û)
3.ƒ≥‘™ÀÿR£¨∆‰‘≠◊”Ω·ππ÷–M(µ⁄3)≤„µÁ◊” ˝ «L(µ⁄2)≤„µÁ◊” ˝µƒ3/4£¨‘Ú∏√‘™Àÿµƒ¿Î◊”Ω·ππ æ“‚Õº «(°°°° )

Àº¬∑Ω‚Œˆ£∫∏˘æð∫ÀÕ‚µÁ◊”≈≈≤ºø…÷™£¨∏√‘≠◊”µ⁄»˝≤„µÁ◊” ˝Œ™8°¡(3/4)=6°£”¶∏√µ√µΩ2∏ˆµÁ◊”°£
¥∞∏£∫B
2.∏˙Ôß∏˘¿Î◊”(NH+4)æþ”–œýÕ¨÷ ◊” ˝∫ÕµÁ◊” ˝µƒ¡£◊” «(°°°° )
A.H2O°°°°°°°°°° B.LiF°°°°°°°°°°°° C.OH-°°°°°°°°°°°°°°°°°° D.Na+
Àº¬∑Ω‚Œˆ£∫NH+4æþ”–11∏ˆ÷ ◊”£¨10∏ˆµÁ◊”£¨”¶∏√”ÎDœýÕ¨°£
¥∞∏£∫D
1.ƒ≥‘™ÀÿRµƒ‘≠◊”∫À¥¯x∏ˆ’˝µÁ∫…£¨‘ÚR2+µƒ∫ÀÕ‚µÁ◊”◊Ð ˝Œ™(°°°° )
A.x-2°°°°°° B.x+2°°°° C.x°°°° D.ŒÞ∑®»∑∂®
Àº¬∑Ω‚Œˆ£∫‘≠◊”∫ÀµƒµÁ∫… ˝ºı»• ß»•µƒµÁ◊” ˝2£¨º¥Œ™∏√¿Î◊”µƒµÁ◊” ˝°£
¥∞∏£∫A
4.÷ ◊” ˝œýÕ¨°¢∫ÀÕ‚µÁ◊” ˝≤ªÕ¨µƒ¡Ω÷÷¡£◊”£¨À¸√«ø…ƒÐ «(°°°° )
A.¡Ω÷÷≤ªÕ¨‘™Àÿµƒ‘≠◊”°°°°°°°°°°°°°°°° B.Õ¨÷÷‘™Àÿµƒ‘≠◊”∫Õ¿Î◊”
C.≤ªÕ¨÷÷‘™Àÿµƒ‘≠◊”∫Õ¿Î◊”°°°°°°°°°°°° D.“ª÷÷∑÷◊”∫Õ“ª÷÷¿Î◊”
Àº¬∑Ω‚Œˆ£∫¡Ω÷÷≤ªÕ¨‘™Àÿµƒ‘≠◊”£¨∆‰÷ ◊” ˝“ª∂®≤ªµ»£¨π A≤ª—°£ªÕ¨÷÷‘™Àÿµƒ‘≠◊”∫Õ¿Î◊”£¨÷ ◊” ˝±ÿ»ªœýÕ¨∂¯∫ÀÕ‚µÁ◊” ˝“ª∂®≤ªÕ¨£¨π B’˝»∑£ª≤ªÕ¨÷÷‘™Àÿµƒ‘≠◊”∫Õ¿Î◊”£¨∆‰÷ ◊” ˝±ÿ»ª≤ªÕ¨£¨π C≤ª—°°£“ª÷÷∑÷◊”∫Õ“ª÷÷¿Î◊”ÕÍ»´”–ø…ƒÐ£¨¿˝»ÁO2∑÷◊”£¨∆‰÷ ◊” ˝Œ™16£¨∫ÀÕ‚µÁ◊” ˝“≤Œ™16£¨∂¯S2-µƒ÷ ◊” ˝Œ™16£¨µ´∆‰∫ÀÕ‚µÁ◊” ˝Œ™18£¨œ‘»ªD’˝»∑°£
¥∞∏£∫BD
10∑÷÷”—µ¡∑ («øªØ¿ý—µ¡∑£¨ø…”√”⁄øŒ÷–)
3.œ¬¡–¡£◊”Ω·ππ æ“‚ÕºƒÐ±Ì æ‘≠◊”µƒ «_________£ª±Ì æ—Ù¿Î◊”µƒ «_________£ª±Ì æ“ı¿Î◊”µƒ «_________°£

Àº¬∑Ω‚Œˆ£∫‘≠◊”Ω·ππ æ“‚Õº÷– £¨ª°œþ±Ì æµÁ◊”≤„£¨ª°œþ…œ√ʵƒ ˝◊÷±Ì æ∏√≤„µƒµÁ◊” ˝£ªµ±÷ ◊” ˝=∫ÀÕ‚µÁ◊” ˝ ±£¨Œ™‘≠◊”µƒΩ·ππ æ“‚Õº£ª÷ ◊” ˝>∫ÀÕ‚µÁ◊” ˝ ±£¨ «—Ù¿Î◊”µƒΩ·ππ æ“‚Õº£ª÷ ◊” ˝<∫ÀÕ‚µÁ◊” ˝ ±£¨ «“ı¿Î◊”Ω·ππ æ“‚Õº°£
£¨ª°œþ±Ì æµÁ◊”≤„£¨ª°œþ…œ√ʵƒ ˝◊÷±Ì æ∏√≤„µƒµÁ◊” ˝£ªµ±÷ ◊” ˝=∫ÀÕ‚µÁ◊” ˝ ±£¨Œ™‘≠◊”µƒΩ·ππ æ“‚Õº£ª÷ ◊” ˝>∫ÀÕ‚µÁ◊” ˝ ±£¨ «—Ù¿Î◊”µƒΩ·ππ æ“‚Õº£ª÷ ◊” ˝<∫ÀÕ‚µÁ◊” ˝ ±£¨ «“ı¿Î◊”Ω·ππ æ“‚Õº°£
¥∞∏£∫AD°°B°°C
2.∏˘æ𜬡–∏˜◊È‘™Àÿµƒ‘≠◊”Ω·ππ æ“‚Õº∑÷Œˆ£¨æþ”–œýÀ∆ªØ—ß–‘÷ µƒ“ª◊È «(°°°° )

Àº¬∑Ω‚Œˆ£∫‘™Àÿµƒ–‘÷ £¨Ãÿ± «ªØ—ß–‘÷ ”Α≠◊”µƒ◊ÓÕ‚≤„µÁ◊” ˝πÿœµ√Ы–£¨◊ÓÕ‚≤„µÁ◊” ˝œýÕ¨£¨∆‰ªØ—ß–‘÷ œýÀ∆£¨◊ÓÕ‚≤„µÁ◊” ˝Œ™8(»Ù÷ª”–1∏ˆµÁ◊”≤„£¨∆‰µÁ◊” ˝Œ™2)£¨∆‰ªØ—ß–‘÷ œý∂‘Œ»∂®°£π A÷–¡Ω÷÷¡£◊”∂º «Œ»∂®Ω·ππ£¨ªØ—ß–‘÷ œýÀ∆°£C÷–æ°πÐ◊ÓÕ‚≤„µƒµÁ◊” ˝∂ºŒ™2£¨µ´«∞’þ «Œ»∂®Ω·ππ£¨∫Û’þ“◊ ß»•2∏ˆµÁ◊”°£
¥∞∏£∫A
1.∞¥“™«Û”√’˝»∑µƒªØ—ß∑˚∫≈±Ì æ£∫
(1)2∏ˆµ™‘≠◊”____________°£(2)Ôß∏˘¿Î◊”____________°£(3)µÿø«÷–∫¨¡ø◊Ó∂ýµƒΩ Ù‘™Àÿ°£____________ (4)1∏ˆ¡ÚÀ·∑÷◊”____________°£(5)ππ≥…¬»ªØƒ∆æßõƒ“ı¿Î◊”____________°£(6)”…¡Ú¿Î◊””Η«Ã˙¿Î◊”ππ≥…µƒŒÔ÷ ____________°£
Àº¬∑Ω‚Œˆ£∫±æÂøº≤Ȫ˘±æªØ—ß∑˚∫≈º∞∆‰”¶”√°£
¥∞∏£∫(1)2N°°(2)NH+4°°(3)Al°°(4)H2SO4°° (5)Cl-°°(6)FeS
19£ÆÕ∆π„ π”√∫¨10%““¥ºµƒ∆˚”Õ£¨ƒøµƒ «ø™∑¢ Ø”ÕÃÊ¥˙◊ ‘¥£¨∏ƒ…∆∆˚≥µŒ≤∆¯≈≈∑≈£Æ≥£Œ¬œ¬£¨““¥º «“ª÷÷ƒÐ»Ð”⁄ÀÆ∫Õ∆˚”Õµƒ“∫㨃Б⁄ø’∆¯÷–»º…’£Æ÷∆»°““¥ºµƒ∑Ω∑® «Ω´µÌ∑€ÀÆΩ‚…˙≥…∆œÃ—ë(ªØ—ß Ω£∫C6H12O6)£¨∆œÃ—ë‘⁄√∏µƒ◊˜”√œ¬◊™ªØŒ™““¥º(ªØ—ß Ω£∫C2H5OH)∫Õ∂˛—ıªØú£¨¡Ì≤È◊ ¡œ÷™£∫÷Ω’≈µ»∫¨œÀŒ¨ÀÿµƒŒÔ÷ “≤ø…ÀÆΩ‚…˙≥…∆œÃ—ë£Æ«Î∏˘æð…œ ˆ–≈œ¢ªÿ¥œ¬¡–Œ £∫
(1)◊ÐΩ·““¥ºµƒ”–πÿ÷™ ∂£Æ““¥ºµƒŒÔ¿Ì–‘÷ ”–£∫______________________________________.““¥ºµƒªØ—ß–‘÷ (”√ªØ—ß∑Ω≥Ã Ω±Ì æ)”–£∫_____________________________________________.
(2)–¥≥ˆ∆œÃ—ë◊™ªØŒ™““¥ºµƒªØ—ß∑Ω≥à Ω:____________________________________________.
(3)»ÙœÎ¿˚”√…̱þµƒ∑œ∆˙ŒÔ…˙≤˙““¥º£¨ƒ„…˜εƒ…˙≤˙π˝≥à «£∫___________________________.
¥∞∏:(1)““¥º «“ª÷÷ƒÐ»Ð”⁄ÀÆ∫Õ∆˚”Õµƒ“∫ÃÂ
C2H5OH+3O2 2CO2+2 H2O
2CO2+2 H2O
(2)C6H12O6 2C2H5OH+2CO2°¸
2C2H5OH+2CO2°¸
(3)∑œ∆˙µƒµÌ∑€¿ýŒÔ÷ (ªÚœÀŒ¨Àÿ¿ýŒÔ÷ )+∆œÃ—ë°˙æ∆æ´£Æ
µ⁄7µ•‘™÷™ ∂Õ¯¬Á
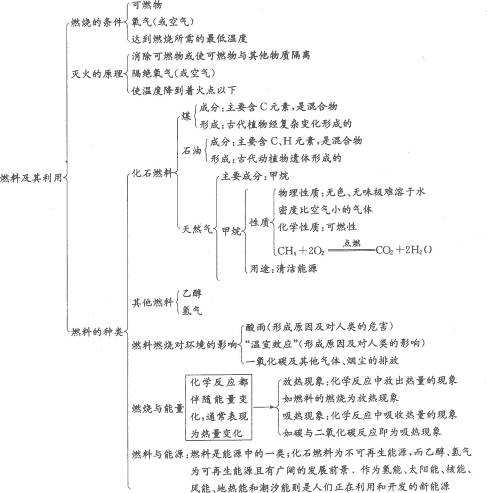
18£Æº◊¥º «“ª÷÷æÁ∂浃°¢æþ”–æ∆æ´∆¯Œ∂µƒ“∫㨜÷∞—“ª∂®÷ ¡øµƒº◊¥º”Î4£Æ4g—ı∆¯ªÏ∫œ”⁄“ª∏ˆ√б’»ð∆˜ƒ⁄£¨µ„»º∑¢…˙»Áœ¬∑¥”¶£∫8CH3OH+xO2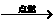 mCO2+nCO+16H2O£Æµ±∑¥”¶ŒÔÕÍ»´◊™ªØŒ™…˙≥…ŒÔ∫Û£¨Ωµ÷¡≥£Œ¬≥£—πœ¬£¨»ð∆˜ƒ⁄”ýœ¬µƒ“∫ÃÂŒ™3£Æ6g£¨«Û£∫
mCO2+nCO+16H2O£Æµ±∑¥”¶ŒÔÕÍ»´◊™ªØŒ™…˙≥…ŒÔ∫Û£¨Ωµ÷¡≥£Œ¬≥£—πœ¬£¨»ð∆˜ƒ⁄”ýœ¬µƒ“∫ÃÂŒ™3£Æ6g£¨«Û£∫
(1)ªØ—ߺ∆¡ø ˝m”Înµƒ∫Õ£ª
(2)∑¥”¶≤˙…˙CO2µƒ÷ ¡ø£ª
(3)œµ ˝xµƒ÷µ£Æ
¥∞∏:(1)8°° (2)3£Æ3 g°° (3)11
÷–øº¡¥Ω”
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com