
题目列表(包括答案和解析)
4.质量为m的三价金属R与稀盐酸反应生成质量为a的氢气,测得金属R的质量减轻了n,金属R的相对原子质量为_________________.
答案:3n/a
基础巩固
3.在反应2A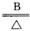 2C+3D中,已知A、B、C的相对分子质量分别为122.5,87,74.5,则D的相对分子质量为__________________________.
2C+3D中,已知A、B、C的相对分子质量分别为122.5,87,74.5,则D的相对分子质量为__________________________.
答案:32
2.等质量的碳、镁、铁分别在足量的氧气中充分燃烧,消耗氧气的质量比是 ( )
A.1∶4∶7 B.6∶3∶4 C.7∶4∶1 D.28∶7∶4
答案:D
1.3g镁在足量的氧气中燃烧,高温可得白色固体的质量为 ( )
A.6 g B.5 g C.10 g D.15 g
答案:B
20.(2010,厦门)某钙片的标签如表6-4,且知此钙成 表6-4
分中只有碳酸钙含有钙元素.
(1)请通过计算说明此标签中的含钙量是错误的.
(2)为测定其真实的含钙量,小东每次取10片钙片放入已称量的含足量盐酸的烧杯中,发生化学反应:CaCO3+2HCl====CaCl2+H2O+CO2↑,充分反应后再称取烧杯和剩余物的总质量,小东做了三次实验,数据如表6-5所示:
表6-5
|
物质的质量 |
第1次 |
第2次 |
第3次 |
第4次 |
|
反应前:烧杯+盐酸/g |
22 |
22 |
22 |
22 |
|
10片钙片/g |
8 |
8 |
8 |
8 |
|
反应后:烧怀+剩余物/g |
26.7 |
26.5 |
26.5 |
26.7 |
①请列式计算每片此钙片含碳酸钙的质量.
②请列式计算每片此钙片的含钙量,并建议厂家如何修改标签.
答案: (1)本品若为纯碳酸钙,其含钙量为碳酸钙含钙质量分数40%,每片含钙量为0.32g,因此本品每片不可能含钙0.75g.
(2)①设:10片钙片含碳酸钙的质量为x,x=7.5g,每片此钙片含碳酸钙0.75g
②每片此钙片的含钙量:0.75g×40%=0.3g建议:将含钙量“每片含钙0.75g”改为“每片含钙0.3 g”.
19.(2010,黄冈)在实验室开放日里,我与小娜、小佳、小华、小丽等同学来到实验室,看到实验桌上摆放着四瓶无标签的试剂,分别是两瓶固体和两瓶液体,我们决定对“固体与液体之间的反应”进行一系列探究.
(1)小娜同学从一瓶固体和一瓶液体中各取少量试剂于试管中进行混合,立即产生了一种五色气体.对气体是何物质,同学们进行了大胆的猜想.小佳同学的猜想可能是
①_____________________________;②_____________________________;……
 (2)我想设计一个实验证明小佳同学猜想①是正确的,实验设计如表6-3(请填写).
(2)我想设计一个实验证明小佳同学猜想①是正确的,实验设计如表6-3(请填写).
表6-3
|
实验步骤 |
现象及结论 |
|
|
|
图6-9
(3)小华想用图6-9给定的收集装置收集一瓶小佳同学猜想②中的气体,则气体由_______________(填a或b)端进入.
(4)小丽同学从另外两瓶试剂中各取少量试剂于试管中,发现混合后,固体发生了变化,但无气泡放出.同学们对加入试管中的固体和液体从不同的反应类型、物质类别等方面进行了大胆的猜想:
猜想一:________________________________________________________________________;
猜想二;________________________________________________________________________;
……
答案:(1)①CO2 ②H2 [或O2等]
(2)如①是CO2 [或H2,或O2等],填表如表D6-1
表D6-1
|
实验步骤 |
现象及结论 |
|
将气体通入澄清石灰水中[将试管口堵一会儿,点燃此气体,或将带火星的木条插入试管中等] |
石灰水变浑浊,则证明是二氧化碳.[或能燃烧,产生淡蓝色火焰,或听到爆鸣声,则证明是氢气,或木条复燃,证明是氧气等] |
(3)②中如果是氢气填a(如是氧气或二氧化碳填b)
(4)猜想一:金屑与盐溶液发生置换反应;猜想二:金属氧化物与酸溶液反应,猜想三:喊与酸溶液发生复分解反应;猜想四,氧化物(如CaO)与水发生化合反应;猜想五:可溶于水的固体物质;猜想六:……
|
执行标准:GBl413-99 主要成分:碳酸钙 含钙量:每片含钙0.75g,每瓶50片,重40g(中外合资××公司出品) |
18.在Na2S、Na2SO3和Na2SO4的混合物中氧的质量分数为22%,则钠元素的质量分数为多少?
答案:28.4% 从Na2S、Na2SO3和Na2SO4的组成上找出Na和S的原子个数比相同,亦即三种物质中Na与S元素的质量比相同,因而三种物质的化合物中Na与S元素的质量比为23×2:32,再根据混合物中O的质量分数求出Na和S的质量分数,从而求得Na的质量分数.
中考链接
17.托盘天平两边各放一只装有稀盐酸的烧杯(盐酸足量)使天平保持平衡.在左边烧杯中加入5g碳酸钙,使其充分反应.应向右边烧杯中投入多少克镁粉,充分反应后天平仍然保持平衡?(已知:Mg+2HCl=MgCl2+ H2
答案:3.05克
16.已知氢气是最轻的气体单质,难溶于水.图6-8所示的装置(正立放置),既用作排水法收集氧气或氢气,又能用作排空气法收集氢气或二氧化碳,试分别简要加以说明,并指明气体流入和流出的方向.
(1)排水法收集氧气:_____________________________________________________________;
(2)排水法收集氢气:_____________________________________________________________;
(3)排空气法收集氢气:___________________________________________________________;
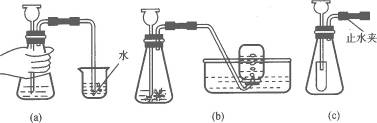
图6-7
(4)排空气法收集二氧化碳:_______________________________________________________.
答案:(1)集气瓶应先装满水,因为氧气不易溶于水,且密度比水小,故气体应从b通入,水从a排出 (2)集气瓶应先装满水,因为氢气难溶于水,且密度比水小,故气体应从b通入,水从a排出 (3)因为氢气密度比空气小,故气体应从b通入,空气从a排出
(4)因为二氧化碳密度比空气大,故气体应从a通入,空气从b排出
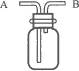
图6-8
15.小明在实验室里学习制取CO2(见图6-7),他的具体操作步骤如下:
(1)组装仪器后进行装置的气密性检查,见图(a).请你帮助他判断,该装置是否漏气?
_________________________________.
(2)他从稀硫酸和稀盐酸中选择一种酸,与石灰石反应制取CO2想一想他不用另外一种酸的理由_________________________________________________.
(3)小明想用图(b)装置制取二氧化碳,你认为是否理想______________,原因是___________________________.
(4)请你告诉他收集满二氧化碳的集气瓶,应该______________(填“正”或“倒”)放在桌面.
(5)小明将气体发生装置稍作改动如图(c),该装置与(a)中发生装置相比,优点是__________________________________________,图中小试管的作用是__________________________________________.
(6)请帮助小明检验c装置的气密性(简述过程)_______________________________________
______________________________________________________________________________.
答案:(1)不漏气 (2)反应中产生微溶于水的硫酸钙附着在大理石的周围,阻止反应继续进行,得到的二氧化碳很少 (3)不理想 因为二氧化碳溶于水 (4)正 (5)可以控制反应随时发生和停止液封
(6)将止水夹夹紧,从长颈漏斗中注入水浸没漏斗下端管口后,若漏斗内液面不再下降,则装置不漏气.
在图c中,由于长颈漏斗使锥形瓶内外相通.因此,不能按常规检查气密性的方法操作,操作时应形成密封气压.小试管的作用可从防止CO2气体散逸上考虑.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com