
题目列表(包括答案和解析)
3.相对原子质量的概念
国际上以一种________为标准,其他原子的质量跟它相比较所得的比值。
由于电子的质量很小,只相当于质子或中子质量的1/1 836,所以原子的质量主要集中在________上,也就是集中在________和________上。质子和中子跟相对原子质量的标准相比较,均约等于,所以相对原子质量约等于________和________之和。
答案:碳原子质量的1/12 原子核 质子 中子 1 质子数 中子数
疑难突破
怎样理解原子的定义和性质?
剖析:由前面学习的分子、原子知识可知:分子在化学变化中是可以再分的,如当氧化汞在加热时,氧化汞的分子被破坏变成组成氧化汞分子的汞的粒子和氧的粒子,这种在化学变化中不能再分的粒子就是原子。原子也可以直接构成物质,如汞、铁等。原子的定义:原子是化学变化中的最小粒子(由化学方法不能再分)。
原子和分子一样也是体积很小、质量很小,且也处在不断运动中。
问题探究
问题 α粒子是带两个单位正电荷的氦原子。1911年,科学家用一束平行高速运动的α粒子轰击金箔(金原子,核电荷数为79,相对原子质量为197)探究原子结构,请模仿科学家进行实验探究。
探究:发生三种实验现象:
(1)有一小部分α粒子改变了原来的运动路径。原因是α粒子途经金原子核附近时,受到斥力而稍微改变了运动方向。
(2)大多数α粒子不会改变原来的运动方向,原因是α粒子通过时,原子内、原子间有空隙。
(3)极少数α粒子被弹回来,原因是α粒子撞击了金原子核而被弹回或撞击了带正电荷、质量大、体积小的金原子核而被弹回。
典题精讲
例1 下列关于原子核的叙述正确的是( )
A.任何原子核都由质子和中子构成
B.质子数等于中子数
C.原子的质量主要集中在原子核上
D.原子核的体积占整个原子的大部分
思路解析:本题考查原子的内部结构知识。氢原子核没有中子,A是错的;质子数并不一定等于中子数,B也是错的;原子核的体积很小,但原子的质量却集中在原子核上,D是错的。
答案:C
例2 1992年,我国科学家首次发现了汞元素的一种新原子。这种汞原子的相对原子质量为208,核电荷数为80,这种汞原子的核外电子数为( )
A.80 B.128 C.208 D.288
思路解析:在原子中,整个原子是不显电性的,因为核电荷数(即质子数)与电子数所带电荷量相等,电性相反。
答案:B
知识导学
原子尽管很小,用化学方法不能再分,但用其他方法可以再分,因为原子也有一定的构成。
理解原子结构的方法:
可以用形象化的比喻来认识原子内的粒子间的比例。在头脑中初步建立起一个原子模型,需要充分发挥想象力。
就目前的实验手段来说,很难看到原子的内部结构。
原子中各种粒子数之间的关系:
①不同原子,原子核所带的电荷数即核电荷数不同,同种原子核电荷数相同,质子数等于核外电子数,但质子数不一定等于中子数。
②在原子中,质子数与中子数不一定相同;并不是所有的原子中都含有中子。
电子的质量在一定程度上可以忽略不计,一个质子和一个中子的质量大约相等,都约等于一个碳原子质量的1/12。
疑难导析
要说明原子是化学变化中的最小粒子,离开了化学变化,它是否可以再分。原子的性质与分子的性质是否相同。如说明原子的质量和体积如何;原子是否在不断地运动;原子间是否有间隔;由原子直接构成的物质,原子是否也保持着该物质的化学性质。
问题导思
要弄清用一束平行高速运动的α粒子轰击金箔(金原子,核电荷数为79,相对原子质量为197),如果一小部分α粒子改变了原来的运动路径,是否可说明原子有原子核;大多数α粒子不会改变原来的运动方向,是否可说明原子内、原子间有空隙,原子内有相对较大的空间;极少数α粒子被弹回来,是否可说明原子核带正电荷、质量大、体积小。
典题导考
绿色通道
要对构成物质的粒子的性质以及各粒子之间的关系真正理解。因此解题的关键是熟记和理解各理论知识,并学会知识间的融会贯通。在这里要明确物质的质量与构成该物质的粒子之间的关系。物质的质量等于构成该物质的粒子乘以物质中所含有的粒子的个数。
典题变式
下列原子各1×1021个,总质量最大的是( )
A.氧原子 B.铁原子
C.氢原子 D.氯原子
答案:B
绿色通道
记住原子中的两个相等关系:核电荷数=质子数=核外电子数,相对原子质量=质子数+中子数。
典题变式
原子R核外有26个电子,核内有30个中子,它的质子数为_______,相对原子质量约为_______。
答案:26 56
2.构成原子的各种粒子之间的关系
在原子中,一个质子带________,中子不带电,一个电子带________,由于原子核内的质子数与核外的电子数________,但电性________,所以整个原子不显电性。在原子中,原子核所带的电荷数(即核电荷数)由质子决定,所以核电荷数=质子数=________。
不同的原子,________不同,由此可见,________决定了原子的种类。
答案: 一个单位的正电荷 一个单位的负电荷 相等 相反 核外电子数 质子数(或核电荷数) 质子数(或核电荷数)
1.原子构成
原子是________中的最小粒子,是指在________中不可再分,不等于原子不可再分。
原子是由居于原子中心的带________电的________和核外带________电的________构成的,而原子核又可以再分,它是由________和________两种粒子构成的。

答案:化学变化 化学变化 正 原子核 负 电子 质子 中子
3.比较表示铁在氧气中燃烧的三种方式,指出化学方程式与其他两种方式相比,它的优点是:____________________________________。
铁在氧气中燃烧生成四氧化三铁:
铁+氧气 四氧化三铁
四氧化三铁
3Fe+2O2 Fe3O4
Fe3O4
答案:不仅能反映出反应物、生成物和反应条件,还能体现出各物质之间的质量关系
疑难突破
怎样选择化学方程式的配平方法?
剖析:(1)若方程式中反应物和生成物比较简单,用“观察法”。
(2)若一种元素在方程式两边只出现了一次,原子个数不相等且差别较大,求出不相等原子个数的最小公倍数,用“最小公倍数法”。
(3)若左右两边出现次数较多的某种元素的原子一边为奇数,一边为偶数,则用“奇数配偶法”。
问题探究
问题 在我们的日常生活和化学实验中,经常使用酒精为燃料来对物质进行加热。酒精的成分是乙醇(化学式为C2H6O),在空气或氧气中燃烧后都生成水和二氧化碳,同时放出大量热。
(1)如果想知道酒精的组成,你应该如何设计实验方案?
(2)你的实验方案还有哪些问题不能解决?
探究:(1)点燃酒精,在火焰上方罩一冷而干燥的烧杯,烧杯内壁上有水雾生成,说明产物有水,生成水则说明酒精中含氢元素。将烧杯迅速倒转过来,向烧杯中倒入澄清的石灰水,石灰水变浑浊,说明产物有二氧化碳,生成二氧化碳则说明酒精中含碳元素。
(2)因酒精燃烧是与氧气发生了反应,产物水和二氧化碳中的氧元素究竟来自于氧气还是酒精不能确定,该实验还不能确定酒精中是否含有氧元素。
典题精讲
例1 下列化学方程式书写完全正确的是( )
A.Mg+O2====MgO2 B.C+O2====CO2
C.S+O2 SO2↑
D.4P+5O2
SO2↑
D.4P+5O2 2P2O5
2P2O5
思路解析:判断一个化学方程式是否正确,首先看是否符合客观事实,再看是否配平,最后观察反应条件是否齐全和是否多标或漏标“↑”或“↓”。本题选项A中方程式没有配平,选项B没有标反应条件(点燃),选项C中反应物中有氧气,SO2则不能标“↑”。
答案:D
例2 一般化学方程式可用最小公倍数法来配平,但这种方法对有些化学方程式却很难行得通。
CO+______Fe2O3 ______Fe+______CO2
______Fe+______CO2
思路解析:这个化学反应中氧原子存在于多种物质中,用最小公倍数法来配平就有点顾此失彼,不过仔细观察分析、比较,不难看出:1个一氧化碳分子要从Fe2O3中夺1个氧原子变成1个二氧化碳分子,而Fe2O3要失去全部氧原子,也就是着眼于C、O两种元素为一个整体。因此氧化铁分子的3个氧原子需3个一氧化碳分子结合走,同时生成3个二氧化碳分子,即CO和CO2前面的化学计量数都为3。
答案:3CO+Fe2O3 2Fe+3CO2
2Fe+3CO2
知识导学
化学方程式的书写要领歌诀:
左写反应物,右写生成物;
写对化学式,系数来配平;
中间连符号,条件要注清;
生成沉淀气,箭头(↓↑)来标明。
书写化学方程式时要注意:
“↑”或“↓”在两种情况下不能标:一是不能在反应物的气体或固体中标,二是反应物中有气体或固体时,在生成物的气体或固体右边标“↑”或“↓”。
书写化学方程式最常见的错误:
写错化学式,忘记配平,漏注反应条件,标错“↑”或“↓”。
利用观察法配平可归纳为以下韵语:
有氢以氢作标准,
无氢以氧为准线;
氢氧全无找一价,
变单成双求配平;
调整只能改系数,
原子各等即为平;
配平系数有分数,
全式乘2被平整。
利用奇数配偶法配平可归纳为以下韵语:
奇数入手,左右开弓;
跟踪追击,单质告终。
疑难导析
正确书写化学方程式的前提是先清楚每一步的含义,然后才能写出具体的化学方程式。配平方程式时,没必要特别注意运用什么方法,配平是我们的最终目的,往往一个化学方程式的配平需要我们对几种方法进行糅合。
问题导思
题目提供的信息是:酒精在空气或氧气中燃烧后都生成水和二氧化碳。信息目的是告诉我们:根据质量守恒定律可知,化学反应前后元素种类是否变化。生成水,说明酒精中应含哪些元素;生成二氧化碳说明酒精中应含什么元素;因酒精燃烧是与氧气发生了反应,产物水和二氧化碳中的氧元素究竟来自于氧气还是酒精不能确定。
原理既然如此,设计实验证明酒精的组成,我们只需用实验证明水和二氧化碳的生成就可以了:证明水的生成应在酒精火焰的上方罩一冷而干燥的烧杯,看是否出现水雾;证明二氧化碳的生成应用澄清的石灰水,看石灰水是否变浑浊,这两条是同学们普遍知道的规律。
再根据质量守恒定律,乙醇中的什么元素参加反应,为什么不能确定酒精中是否含有氧元素。
典题导考
黑色陷阱
书写化学方程式时常会发生以下错误:①写错反应物或生成物的化学式,不会配平。②未写或写错反应条件、生成物的状态符号(“↑”或“↓”)及位置。③“↑”或“↓”应标在生成物中,且只有反应物中没有气体,而生成物中有气体时用“↑”,反应物中没有固体,而生成物中有固体时用“↓”。
典题变式
下列化学方程式书写正确的是( )
A.H2O2====H2↑+O2↑
B.Fe+O2 Fe3O4
Fe3O4
C.H2+O2 H2O
D. S+O2
H2O
D. S+O2 SO2
SO2
答案:D
绿色通道
化学方程式的配平是指根据质量守恒定律,在化学式前面配上适当的化学计量数,使式子左、右两边的每种元素的原子数目相等。常见的化学方程式的配平方法有三种,即观察法、最小公倍数法和奇数配偶法。
典题变式
配平下列化学方程式:
(1) Fe+Cl2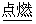 FeCl3
FeCl3
(2)FeS2+O2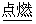 Fe2O3+ SO2
Fe2O3+ SO2
答案:(1)2Fe+3Cl2 2FeCl3
2FeCl3
(2)4FeS2+ 11O2 2Fe2O3+
8SO2
2Fe2O3+
8SO2
2.化学方程式的配平
为使书写的化学方程式遵守__________定律,要在化学方程式两边的化学式的前面配上适当的__________,使化学方程式等号两边各种原子的__________和__________都相同,这个过程叫配平。
正确的化学方程式应当是配平的,反应物和生成物之间用__________连接,还要标明化学反应发生的__________。如果__________中无气体,__________中有气体,在__________的气体符号__________边要注__________号;溶液中的反应,如果生成物中有__________,则在固体物质的化学式的右边要注__________号。
答案:质量守恒 化学计量数 种类 数目 等号 条件 反应物 生成物 生成 右 ↑ 沉淀 ↓
1.化学方程式的书写原则
化学方程式反映化学反应的客观事实。因此,书写化学方程式要遵守两个原则:一是必须__________________,决不能凭空臆想、臆造事实上不存在的物质和化学反应;二是要__________________,等号两边各原子的种类与数目必须相等。
答案:以客观事实为基础 遵守质量守恒定律
3.化合反应与氧化反应
由两种或两种以上的物质生成__________的化学反应,叫做化合反应。如硫、铝在氧气中燃烧就属于化合反应。
物质跟__________发生的反应叫氧化反应。氧化反应是指物质跟氧发生的化学反应,而不是专指物质跟氧气发生的化学反应。物质跟氧气发生的化学反应只是氧化反应的一种形式。
答案:另一种物质 氧
疑难突破
利用高锰酸钾制氧气时怎样检查装置的气密性?
剖析:先把导气管的一端放入水里,然后两手紧贴容器外壁,如果装置不漏气,里面的空气受热膨胀,导管口有气泡冒出。松开两手,使它冷却,导管中就会形成一段水柱。
问题探究
问题 有四个集气瓶,分别充满了空气、氮气、二氧化碳和氧气,试用简单的方法加以鉴别。
探究:把燃着的木条分别伸入四个集气瓶中,木条正常燃烧的原气体是空气;木条燃烧更旺的原气体是氧气;木条火焰熄灭的原气体是氮气和二氧化碳。再向使火焰熄灭的两个集气瓶中加入适量的澄清石灰水并振荡,使澄清石灰水变浑浊的原气体是二氧化碳,没有变化的原气体是氮气。
典题精讲
例1 下列有关氧气实验现象的描述正确的是( )
A.硫在空气中燃烧产生蓝紫色火焰 B.磷在氧气中燃烧产生白色烟雾
C.碳在氧气中燃烧发出白光 D.碳在氧气中燃烧生成二氧化碳
思路解析:硫在空气中和在氧气中燃烧的火焰颜色是不同的,在空气中呈淡蓝色,在氧气中呈蓝紫色。磷在氧气中燃烧产生白烟,因为生成物五氧化二磷是白色固体。“碳在氧气中燃烧生成二氧化碳”不是对实验现象的描述。
答案:C
例2 下列性质属于化学性质的是( )
A.氧气不易溶于水 B.氮气是没有颜色、没有气味的气体
C.镁带能在空气中燃烧 D.汽油易挥发
思路解析:发生化学变化才能表现出来的性质是化学性质。C项是因“镁在空气中燃烧生成了新物质氧化镁”才表现出的性质,所以是化学性质。
答案:C
知识导学
学习氧气时注意:
①由于氧气的密度比空气大,所以氧气在收集时可用向上排空气法;又由于氧气不易溶于水,所以氧气可用排水法收集。
②水中的生物是依靠溶解在水中的氧气生存的。
③氧气在气态时是无色的,在固态和液态时是淡蓝色。
描述物质在氧气中燃烧现象的方法:
重点是描述木炭、硫、铝、磷、铁等在氧气中燃烧的实验现象,描述物质在氧气中燃烧的现象时,一般从四方面来描述:①物质原来的颜色;②对产生的光(火焰或火星)加以描述;③放出热量;④对生成物加以描述。
进行实验时要注意的问题:
①夹木炭的坩埚钳由上而下慢慢伸入瓶中,如果很早伸入集气瓶的底部,瓶中的氧气被热的气体赶出来,木炭燃烧会不旺。
②硫的用量不能过多,防止对空气造成污染,实验时应在通风橱中进行。
③光一般指固体燃烧产生的现象,如镁条燃烧、木炭燃烧等只产生光,不产生火焰;火焰是指气体燃烧或固体或液体的蒸气燃烧产生的现象。
④五氧化二磷是固体,现象应描述为产生白烟。烟是指固体小颗粒,雾是指液体小液滴。
⑤细铁丝绕成螺旋状;铁丝一段系一根火柴;集气瓶内预先装少量水或铺一层细砂。
⑥蜡烛燃烧时盛氧气的集气瓶要干燥,可观察到水雾。
理解缓慢氧化要注意:
缓慢氧化是指进行很缓慢的氧化反应,也要放出热量。如果放出的热量使温度达到可燃物的着火点,就可以引起自发燃烧,也就是自燃。缓慢氧化也可以向剧烈氧化反应转化。
供给呼吸氧主要用于:医疗、登山、潜水、宇航;支持燃烧氧主要用于:炔焰用于焊接和切割,炼钢,作火箭助燃剂。
化合反应特征的记忆方法:
可概括为:“多变一”,可用通式A+B+……→AB……来表示。
学习化合反应与氧化反应时易出现的认知误区:
化合反应不一定是氧化反应,氧化反应也不一定是化合反应,两者没有必然的联系。
疑难导析
要说明检查装置的气密性关键是先后顺序一定不能颠倒;然后说明怎样连接仪器,如何操作;最后说明要注意什么问题,否则会造成怎样的结果。
问题导思
此题属于物质的鉴别题,做鉴别题的原则是:?①找出题目中所给物质中有特性的物质,依据特性作为解题的突破口,再依次鉴别;②步骤要少,现象要明显;③叙述要明朗清晰,按操作--现象--结论的程序论述,不可先说结论后说现象;④操作要简便可行。
典题导考
对于描述物质在氧气中燃烧时的现象,应该在做试验时仔细观察现象,并对物质在空气中和在氧气中燃烧的现象作出比较,熟练记忆。
典题变式
下列实验现象的描述正确的是( )
A.铁丝在氧气中燃烧时,火星四射,生成黑色固体
B.红磷在空气中燃烧时,产生大量的白雾
C.木炭在氧气中燃烧时,发出白色火焰
D. 硫在空气中燃烧产生蓝紫色火焰
答案:A
绿色通道
判断物质的性质是物理性质还是化学性质,关键看是否发生化学变化并通过化学变化表现出来。
典题变式
下列物质的用途,主要利用化学性质的是( )
A.铜制作导线
B.活性炭吸附冰箱中的异味
C.氧气供给呼吸
D.稀有气体作为霓虹灯的填充气
答案:CD
2.氧气的用途
(1)供给__________。
(2)支持__________。
答案:呼吸 燃烧
1.认识氧气的性质
(1)氧气的物理性质
通常状况下,氧气是一种__________、__________的气体,密度稍__________空气,氧气__________溶于水,通常状况下,1 L水中能溶解30 mL氧气。
氧气有三态变化,在加压降温时,氧气可变成__________色的液体,甚至可变成雪花状__________色的固体。
(2)氧气的化学性质
|
反应物 |
在氧气中的燃烧现象 |
反应表达式 |
|
木炭(灰黑色固体) |
①在空气中燃烧发出红光。②在氧气中燃烧发出________。③放出________。④生成的气体能使________ |
碳+氧气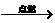 ________ ________C+O2 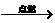 CO2 CO2 |
|
硫(淡黄色固体) |
①在空气中燃烧发出________。②在氧气中燃烧发出明亮的________。③放出________。④生成有________气味的气体 |
硫+氧气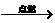 ________ ________S+O2 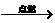 ________SO2 ________SO2 |
|
磷(暗红色) |
①红磷燃烧产生浓厚________。②在空气中燃烧产生黄色光。③在氧气中燃烧发出耀眼的________。④放出________ |
磷+氧气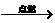 P+O2 P+O2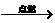 P2O5 P2O5 |
|
铁(银白色) |
①剧烈燃烧。②________。③放出________。④生成________ |
铁+氧气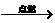 ________ ________Fe+O2 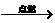 Fe3O4 Fe3O4 |
|
蜡烛(白色固体) |
①火焰明亮,发出________。②放出________。③瓶壁上有________出现。④生成能使________的气体 |
石蜡+氧气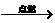 ________+________ |
小结:氧气是一种化学性质比较__________的气体,许多物质可与氧气发生反应。在某些条件下,物质与氧气的反应比较剧烈;而在另一些条件下,物质与氧气发生缓慢的氧化反应,如动植物的新陈代谢、金属器皿的锈蚀、食物的腐烂、有机肥的腐熟等变化过程都包含有__________作用。
答案:(1)无色 无味 大于 不易 淡蓝 淡蓝
(2)白光 热量 澄清石灰水变浑浊 二氧化碳
微弱的淡蓝色火焰 蓝色火焰 热量 刺激性 二氧化硫
白烟 白光 热量 五氧化二磷
白光 热量 白色固体 三氧化二铝(氧化铝)
火星四射 热量 黑色固体 四氧化三铁
明亮白光 热量 水珠 澄清石灰水变浑浊 二氧化碳 水
活泼 缓慢氧化
2.为什么烧水的水壶内时间长了会有水垢?
剖析:因为水中含有可溶性的钙、镁化合物,在烧水的过程中,温度升高,发生化学变化,形成不溶性的物质,即形成了水垢。
问题探究
问题1 家中的水壶使用较长一段时间后,在壶底会结上一层厚厚的水垢(它的主要成分是碳酸钙与氢氧化镁,能溶于酸)。试利用家中现有的物质和用品设计一个实验来除去铝壶中的水垢。
探究:水垢能溶于酸,家中常见的酸,就是醋酸。先用机械刮擦的方法除去壶帮和壶嘴里比较松软的水垢,这样可以减少食醋的用量,然后把食醋倒入壶里。为了加快反应,还应该把水壶加热,温度维持在60-70℃。这样,水垢就可以慢慢变得疏松,容易去除。
问题2 设计实验区分蒸馏水和自来水。
探究:取这两种水各少许放于两个烧杯中,加热蒸发至完全没有,观察烧杯底部,如果出现少量的固体物质则是自来水,另一种水则为蒸馏水。
典题精讲
例1 在日常生活中,有人喜欢喝纯净水,市售纯净水中有一些是蒸馏水,有关这类纯净水的下列说法中,正确的是( )
A.它是纯天然饮品,不含任何化学物质
B.它是一种硬水
C.它在通电条件下不能分解成氢气和氧气
D.它纯净、清洁,但不宜长期饮用
思路解析:蒸馏水是纯水,不含矿物离子和微量元素,不适合饮用;但它是化合物,本身就是化学物质,不能说不含化学物质;通电时能够电解,生成氢气和氧气,但电解很慢;它洁净,是纯水,但不适合做饮用水水源。
答案:D
例2 通电分解水的简易装置如图3-11所示。
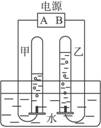
图3-11
(1)在水中加入少量硫酸或氢氧化钠的目的是为了_______________________________。
(2)试管甲中生成的是_______气,则B极为_______极(填“正”或“负”),甲、乙两试管内气体的质量比为_______。
(3)电解水的实验说明水是由_______组成的。这个实验还验证了在化学反应里_______,可以分成原子,而_______不能再分。
思路解析:由于纯水的导电性能很差,应该加入酸或碱增强水的导电性,使电解加快。水电解生成氢气和氧气,说明水是由氢元素和氧元素组成的。电解过程把水分子变成氢、氧原子,说明原子是化学变化中的最小粒子。
答案:(1)增强水的导电性,加快电解速度
(2)氢 正 1∶8
(3)氢、氧 分子可以再分 原子
知识导学
在压强为101 kPa时,水加热到100 ℃就烧开了。冬天,到了0 ℃就要结冰。冰浮在水面上。
利用明矾等絮凝剂溶于水后,生成的胶状物对杂质进行吸附,使杂质沉降来达到净水的目的。
过滤时要注意:
过滤是分离混合物的一种常用的方法。若两种物质混合,需进行过滤分离,则必须符合一种可溶,一种不溶。过滤时一定严格按照“一贴”“二低”“三靠”进行操作。否则,容易导致实验失败。
几种水净化方法的比较:
|
水的净化方法 |
除去不溶性杂质 |
除去可溶性杂质 |
降低水的硬度 |
|
静置沉淀 |
可以 |
否 |
|
|
过滤 |
可以 |
否 |
|
|
吸附 |
可以 |
可以 |
|
|
蒸馏 |
可以 |
可以 |
可以 |
蒸馏操作时要注意的要点:
①在烧瓶中加入约1/3体积的硬水,再加入少量防暴沸沸石或碎瓷片。
②蒸馏时注意保持温度缓慢上升,同时通入冷水进行冷却。
③当蒸馏烧瓶中只有少量液体或已达到规定要求时即停止蒸馏。
人们长期饮用硬水有害人体的健康。
水垢形成的原理:
人们在煮沸硬水的过程中,可以看到形成水垢,水垢的形成主要是因为原来可溶性的钙、镁化合物经过加热后,形成了不溶性的化合物。水垢的主要成分是碳酸钙和氢氧化镁。
蒸馏水是净化程度较高的水。
疑难导析
需说明水中的杂质有哪些,无色透明的水是否一定不含可溶性杂质,可溶性杂质是否一定对人体健康有利。
要说明水中含有什么物质,这些物质在加热时会发生什么变化,生成什么物质。
问题导思
要先知道水垢的成分,在家中什么物质能与之反应。
为了减少酸的用量,先用什么办法除垢,要说明水中含有什么物质,这些物质在加热时会发生什么变化,对反应有何影响,生成什么物质,水垢怎样变化,是否容易除去。
先要知道蒸馏水是否是纯度较高的水,有无不溶性杂质,有无可溶性杂质。自来水中有无不溶性杂质,有无可溶性杂质,然后把水蒸发除去,可溶性杂质亦即可暴露出来。根据蒸馏水和自来水的现象不同即可判断。
典题导考
绿色通道
物质的外观与物质的本质有很大的差距,我们不能凭视觉效果判断物质的组成或推测物质的性质,必须利用实验分析物质的组成。
典题变式
下列说法正确的是( )
A污水只是看起来脏点,其实没有害处
B.水厂的水源不需要选择
C.污水里有病菌
D.农村空气好,没有污水
答案:C
绿色通道
电解过程增强导电性的方法是加入电解质;加入的一般是硫酸或氢氧化钠。不要以为加入任意酸、碱都可以,有的酸会对电解产生影响。
典题变式
电解54 g水,可得到氢气( )
A.6 g B.3 g C.1.5 g D.8 g
答案:A
典题变式
电解水时常加入少量的稀硫酸或氢氧化钠溶液是因为( )
A.它们是水分解反应的催化剂
B.可以增强水的导电性
C.可以更多地生成氢气和氧气
D.可以用它们除掉水中的有害物质
答案:B
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com