
题目列表(包括答案和解析)
4.(1)A、B(2)非金属;因为A+B→乙+C,且乙为单质,可知乙元素在A、B中分别显正、负价,所以乙是非金属。(3)S(或N2)H2S(或NH3)
7.(1)C+H2O(气)→CO+H2(2)NH4++H2O→NH3·H2O+H+
(3)尿素H4NOOC-COONH4(4)3CuO+2NH3→3Cu+N2+3H2O
8答案:硫酸、淀粉-碘化钾试纸淀粉-碘化钾试纸变蓝色。酸性高锰酸钾溶液,高锰酸钾溶液的紫色消失。
课后习题
|
1A |
2A |
3C |
6.(1)(NH4)2S O2 H2O(2)H2SO4 (3)HNO3
5.在化工生产中,要用到一种无色、可溶于水的晶体:铝铵矾。该晶体是一种复盐,其主要成分是十二水合硫酸铝铵。向该复盐的浓溶液中逐滴加入浓NaOH溶液,将发生一系列变化。
NH4+ +Al3+ +H2O→Al(OH)3↓+NH3↑
试回答:
(1)硫酸铝铵在水溶液中的电离方程式为___ ___;
(2)在逐滴加入浓NaOH溶液的过程中,产生的现象有:①溶液中出现白色沉淀;②有刺激性气味的气体产生;③白色沉淀量逐渐增多;④白色沉淀完全消失;⑤白色沉淀量逐渐减少。
请答出各种现象由先到后出现的顺序(用序号回答)____→____→____→____→____;
(3)写出滴入NaOH溶液的过程中,有关反应的离子方程式:①____;②______;③____。
专题(八) 非金属元素答案
例1Ge:第Ⅳ主族元素,最高正价+4;最高价氧化物GeO2。
Bi:第Ⅴ主族元素,最外层5个电子→满足8电子稳定结构应形成共价键数目:8-5=3→BiCl3→在BGO中铋为+3价→氧化物Bi2O3。
设BGO化学式为mGeO2·nBi2O3
有:2m=3n m∶n=3∶2 m=3 n=2
→BGO化学式为3GeO2·2Bi2O3 (或Bi4(GeO4)3)
例2答案:(1)H3PO4(2)2种(化合与复分解),5(3)O(O2与O3)、P(红磷与白磷)例3答案:(1)H2(2)2F2+2H2O→4HF+O2↑
(3)若D为N2,丙、丁分别是NH3和NO,在一定条件下可以反应(NH3、NO中N元素的化合价分别是-3、+2,0价居其中);若D为C,丙、丁分别是CH4与CO2,化合价分别是-4、+4,0价居其中,故理论上也可发生反应生成碳单质。
课堂练习
|
1A |
2C |
3C |
4B |
5D |
4.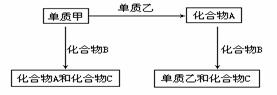 A、B、C是中学化学常见的三种化合物,它们各由两种元素组成,甲、乙是两种单质,这些化合物和单质之间存在如下的关系:
A、B、C是中学化学常见的三种化合物,它们各由两种元素组成,甲、乙是两种单质,这些化合物和单质之间存在如下的关系:
据此判断:
(1)在A、B、C这三种化合物中,必定含有乙元素的是____(用A、B、C字母填写)。
(2)单质乙必定是____(填“金属”或“非金属”),其理由是__ __
(3)单质乙的化学式可能是____,则化合物B的化学式是____。
3.下列有关工业生产的叙述中, 错误的是 ( )
A.制普通玻璃的主要原料是纯碱、石灰石、石英
B.氨是制作氮肥、硝酸、铵盐的重要原料
C.将二氧化硫催化氧化成三氧化硫后, 在吸收塔内用水吸收制得浓硫酸
D.炼铁的主要原理是在高温下, 用还原剂从铁矿石把铁还原出来
2.下列物质间发生化学反应:①H2S+O2,②Na+O2,③Cu+HNO3,④P2O5+H2O,⑤Fe+HCl。在不同条件下得到不同产物的是 ( )
A.①②③④ B.①③⑤ C.②③④⑤ D.①②③④⑤
1.汽车尾气中的CO、NO都是城市空气中浓度较高的严重污染物,有关它们
的叙述不正确的是
A.CO、NO的燃烧产物分别是CO2和NO2
B.NO、NO2的混合气可与水反应生成一些HNO2,但NO、NO2都不是HNO2的酸酐
C.化学上有一种说法:等电子体结构类似。CO与NO+(亚硝酰基阳离子)的微粒中最外层电子数之和相等,应具有类似的结构
D.在催化剂作用下,可通过反应:2CO+2NO→N2+2CO2来达到净化汽车尾气的目的
8.某学生设计实验,欲选用下列试剂证明NaNO2既有氧化性,又有还原性。
试剂:酸性高锰酸钾溶液、硝酸、硫酸、碘单质、淀粉-碘化钾试纸。
回答:欲证明NaNO2的氧化性,所选用的试剂是__ ____,观察到的现象是_ ____。
欲证明NaNO2的还原性,所选用的试剂是__ ____ ,观察到的现象是___ ___。
[课后习题]
7.已知A、B、C、D是短周期中的4种非金属元素,它们的原子序数依次增大。A元素原子形成的离子就是一个质子。又知,①B单质在高温下可从A与D组成的某种化合物中置换出A,同时生成化合物BD,②A、C、D三种元素组成的某种盐水溶液显酸性,③B、C均能与D组成原子数比为1∶1和1∶2的化合物。
(1)写出①中反应的化学方程式__ ____,
(2)写出②中盐的水溶液显酸性的原因(写出离子方程式)___ ___,
(3)这四种元素可组成原子个数比4∶1∶2∶1(按A、B、C、D顺序)的化合物,其名称为__ __。这四种元素又可组成原子个数比为4∶1∶1∶2(按A、B、C、D顺序)的化合物,其结构简式为__ ____,
(4)C元素的气态氢化物能还原CuO,生成Cu、C单质及A与D形成的化合物,该反应的化学方程式为_ _____。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com