
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
‘À”√ªØ—ß∑¥”¶‘≠¿Ì—–æøµ™°¢¡Ú°¢¬»°¢µ‚µ»µ•÷ º∞∆‰ªØ∫œŒÔµƒ∑¥”¶”–÷ÿ“™“‚“°£
£®1£©¡ÚÀ·…˙≤˙÷–£¨SO2¥þªØ—ıªØ…˙≥…SO3£∫![]()
![]() ªÏ∫œÃÂœµ÷–SO3µƒ∞Ÿ∑÷∫¨¡ø∫ÕŒ¬∂»µƒπÿœµ»Áœ¬ÕºÀ˘ 森«˙œþ…œ»Œ∫Œ“ªµ„∂º±Ì æ∆Ω∫‚◊¥Ã¨£©°£∏˘æðÕº æªÿ¥œ¬¡–Œ £∫
ªÏ∫œÃÂœµ÷–SO3µƒ∞Ÿ∑÷∫¨¡ø∫ÕŒ¬∂»µƒπÿœµ»Áœ¬ÕºÀ˘ 森«˙œþ…œ»Œ∫Œ“ªµ„∂º±Ì æ∆Ω∫‚◊¥Ã¨£©°£∏˘æðÕº æªÿ¥œ¬¡–Œ £∫
 ¢Ÿ
¢Ÿ![]() µƒ°˜H°°°°°°°°0£®ÃÓ°∞>°±
µƒ°˜H°°°°°°°°0£®ÃÓ°∞>°±
ªÚ°∞<°±£©£ª»Ù‘⁄∫„Œ¬°¢∫„—πÃıº˛œ¬œÚ…œ ˆ∆Ω∫‚ÃÂœµ÷– Õ®»Î∫§∆¯£¨∆Ω∫‚°°°°°°°°°°“∆∂Ø£®ÃÓ°∞œÚ◊Û°±°¢°∞œÚ”“°±ªÚ°∞≤ª°±£©£ª
¢⁄»ÙŒ¬∂»Œ™T1°¢T2£¨∑¥”¶µƒ∆Ω∫‚≥£ ˝∑÷±Œ™K1°¢K2£¨
‘ÚK1 K2£ª∑¥”¶Ω¯––µΩ◊¥Ã¨D ±£¨V’˝ vƒÊ
£®ÃÓ°∞>°±°¢°∞<°±ªÚ°∞=£©
 £®2£©µ™ «µÿ«Ú…œ∫¨¡ø∑·∏ªµƒ“ª÷÷‘™Àÿ£¨µ™º∞∆‰ªØ∫œŒÔ‘⁄π§≈©“µ…˙≤˙°¢…˙ªÓ÷–”–◊≈÷ÿ“™◊˜”√°£
£®2£©µ™ «µÿ«Ú…œ∫¨¡ø∑·∏ªµƒ“ª÷÷‘™Àÿ£¨µ™º∞∆‰ªØ∫œŒÔ‘⁄π§≈©“µ…˙≤˙°¢…˙ªÓ÷–”–◊≈÷ÿ“™◊˜”√°£
¢Ÿ”“Õº «“ª∂®µƒŒ¬∂»∫Õ—π«øœ¬ «N2∫ÕH2∑¥”¶…˙≥…1molNH3π˝≥Ã÷–ƒÐ¡ø±‰ªØ æ“‚Õº£¨«Î–¥≥ˆπ§“µ∫œ≥…∞±µƒ»»ªØ—ß∑¥”¶∑Ω≥Ã Ω£∫°°°°°°°° °°°££®°˜Hµƒ ˝÷µ”√∫¨◊÷ƒ∏Q1°¢Q2µƒ¥˙ ˝ Ω±Ì æ£©
¢⁄∞±∆¯»Ð”⁄ÀƵ√µΩ∞±ÀÆ°£‘⁄25°„Cœ¬£¨Ω´a mol°§L£≠1µƒ∞±ÀÆ”Î
b mol°§L£≠1µƒ—ŒÀ·µ»Ãª˝ªÏ∫œ£¨∑¥”¶∫ۻГ∫÷–œ‘÷––‘£¨‘Ú£∫
c£®NH+4£© c£®Cl£≠£©£®ÃÓ°∞>°±°¢°∞<°±ªÚ°∞=°±£©£ª”√∫¨a∫Õbµƒ¥˙ ˝ Ω±Ì æ∏√ªÏ∫œ»Ð“∫÷–“ªÀÆ∫œ≥ˆ∞±µƒµÁ¿Î∆Ω∫‚≥£ ˝±Ì¥Ô Ω°°°°°°°°°°°°°°°°°°°°°° °£
£®3£©1000°Ê ±£¨¡ÚÀ·ƒ∆”Ϋ‚∆¯∑¢…˙œ¬¡–∑¥”¶£∫
Na2SO4(s) + 4H2(g) ![]() Na2S(s) + 4H2O(g) °£
Na2S(s) + 4H2O(g) °£
¢Ÿ∏√∑¥”¶µƒ∆Ω∫‚≥£ ˝±Ì¥Ô ΩŒ™____________________°£“—÷™K1000°Ê£ºK1200°Ê£¨‘Ú∏√∑¥”¶ «________∑¥”¶£®ÃÓ°∞Œ¸»»°±ªÚ°∞∑≈»»°±£©°£
¢⁄”√”–πÿ¿Î◊”∑Ω≥à ΩÀµ√˜…œ ˆ∑¥”¶À˘µ√πÃÃÂ≤˙ŒÔµƒÀƻГ∫µƒÀ·ºÓ–‘
£®4£©25°Ê ±£¨“—÷™NH4A»Ð“∫Œ™÷––‘£¨”÷÷™Ω´HA»Ð“∫º”µΩNa2CO3»Ð“∫÷–”–∆¯ÃÂ∑≈≥ˆ£¨ ‘Õ∆∂œ(NH4)2CO3»Ð“∫µƒpH 7£®ÃÓ£º°¢£æ°¢£Ω£©£ªœýÕ¨Œ¬∂»œ¬£¨µ»ŒÔ÷ µƒ¡ø≈®∂»µƒœ¬¡–—Œ»Ð“∫∞¥pH”…¥ÛµΩ–°µƒ≈≈¡–À≥–ÚŒ™ °££®ÃÓ–Ú∫≈£©
a.£ÆNH4HCO3 b£ÆNH4A c£Æ(NH4)2CO3 d£ÆNH4Cl
£®¢Ò£©Ãº∫ÕúµƒªØ∫œŒÔ‘⁄»À¿ý…˙≤˙°¢…˙ªÓ÷–µƒ”¶”√∑«≥£π„∑∫°£°∞µÕú…˙ªÓ°±≤ª‘Ÿ÷ª «“ª÷÷¿ÌœÎ£¨∏¸ «“ª÷÷÷µµ√∆⁄¥˝µƒ…˙ªÓ∑Ω Ω°£
£®1£©º◊ÕÈ»º…’ ±∑≈≥ˆ¥Û¡øµƒ»»£¨ø…◊˜Œ™ƒÐ‘¥”¶”√”⁄»À¿ýµƒ…˙≤˙∫Õ…˙ªÓ°£ 
£®2£©Ω´¡Ω∏ˆ ؃´µÁº´≤»ÎKOH»Ð“∫÷–£¨œÚ¡Ωº´∑÷±Õ®»ÎCH4∫ÕO2£¨ππ≥…º◊ÕÈ»º¡œµÁ≥ÿ°£∆‰∏∫º´µÁº´∑¥”¶ Ω «£∫??????????????????????????? °£
£®3£©Ω´≤ªÕ¨¡øµƒCO£®g£©∫ÕH2O£®g£©∑÷±Õ®»ÎµΩê˝Œ™2Lµƒ∫„»ð√б’»ð∆˜÷–£¨Ω¯––∑¥”¶£∫
 £¨µ√µΩ»Áœ¬»˝◊È ˝æð£∫
£¨µ√µΩ»Áœ¬»˝◊È ˝æð£∫

¢Ÿ µ—È1÷–£¨“‘v£® H2£©±Ì 浃∆Ωæ˘∑¥”¶ÀŸ¬ Œ™£∫???? °£
¢⁄∏√∑¥”¶µƒ’˝∑¥”¶Œ™???? £®ÃÓ°∞Œ¸°±ªÚ°∞∑≈°±£©»»∑¥”¶£ª
¢€»Ù“™ µ—È3¥ÔµΩ”Î µ—È2œýÕ¨µƒ∆Ω∫‚◊¥Ã¨£®º¥∏˜ŒÔ÷ µƒÃª˝∑÷ ˝∑÷±œýµ»£©£¨‘Úa°¢b”¶¬˙◊„µƒπÿœµ « ????? £®”√∫¨a°¢bµƒ ˝—ß Ω±Ì æ£©°£
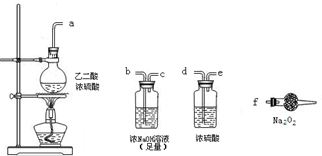
£®¢Ú£©ƒ≥–°◊È‘À”√𧓵…œ¿Î◊”Ωªªªƒ§∑®÷∆…’ºÓµƒ‘≠¿Ì£¨”√»Áœ¬ÕºÀ˘ æ◊∞÷√µÁΩ‚K2SO4»Ð“∫°£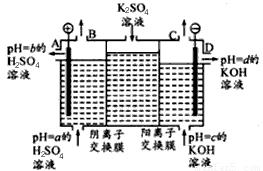
¢Ÿ∏√µÁΩ‚≤€÷–Õ®π˝“ı¿Î◊”Ωªªªƒ§µƒ¿Î◊” ˝?????? £®ÃÓ°∞>°±°∞<°±ªÚ°∞“ª°±£©Õ®π˝—Ù¿Î◊”Ωªªªƒ§µƒ¿Î◊” ˝£ª
¢⁄Õº÷–a°¢b°¢c°¢d∑÷±±Ì æ”–πÿ»Ð“∫µƒpH£¨‘Úa°¢b°¢c°¢d”…–°µΩ¥ÛµƒÀ≥–ÚŒ™ ???????? ?? £ª
¢€µÁΩ‚“ª∂Œ ±º‰∫Û£¨B≥ˆø⁄”ÎC≥ˆø⁄≤˙…˙∆¯Ãµƒ÷ ¡ø±»Œ™?? ????????? °£
£®¢Ò£©Ãº∫ÕúµƒªØ∫œŒÔ‘⁄»À¿ý…˙≤˙°¢…˙ªÓ÷–µƒ”¶”√∑«≥£π„∑∫°£°∞µÕú…˙ªÓ°±≤ª‘Ÿ÷ª «“ª÷÷¿ÌœÎ£¨∏¸ «“ª÷÷÷µµ√∆⁄¥˝µƒ…˙ªÓ∑Ω Ω°£
£®1£©º◊ÕÈ»º…’ ±∑≈≥ˆ¥Û¡øµƒ»»£¨ø…◊˜Œ™ƒÐ‘¥”¶”√”⁄»À¿ýµƒ…˙≤˙∫Õ…˙ªÓ°£ 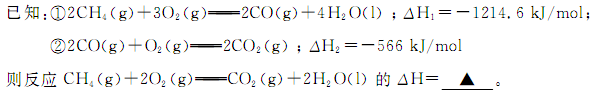
£®2£©Ω´¡Ω∏ˆ ؃´µÁº´≤»ÎKOH»Ð“∫÷–£¨œÚ¡Ωº´∑÷±Õ®»ÎCH4∫ÕO2£¨ππ≥…º◊ÕÈ»º¡œµÁ≥ÿ°£∆‰∏∫º´µÁº´∑¥”¶ Ω «£∫ °£
£®3£©Ω´≤ªÕ¨¡øµƒCO£®g£©∫ÕH2O£®g£©∑÷±Õ®»ÎµΩê˝Œ™2Lµƒ∫„»ð√б’»ð∆˜÷–£¨Ω¯––∑¥”¶£∫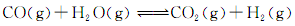 £¨µ√µΩ»Áœ¬»˝◊È ˝æð£∫
£¨µ√µΩ»Áœ¬»˝◊È ˝æð£∫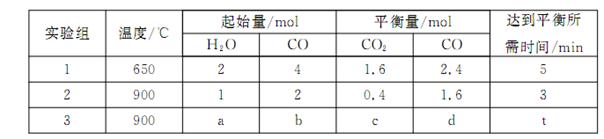
¢Ÿ µ—È1÷–£¨“‘v£® H2£©±Ì 浃∆Ωæ˘∑¥”¶ÀŸ¬ Œ™£∫ °£
¢⁄∏√∑¥”¶µƒ’˝∑¥”¶Œ™ £®ÃÓ°∞Œ¸°±ªÚ°∞∑≈°±£©»»∑¥”¶£ª
¢€»Ù“™ µ—È3¥ÔµΩ”Î µ—È2œýÕ¨µƒ∆Ω∫‚◊¥Ã¨£®º¥∏˜ŒÔ÷ µƒÃª˝∑÷ ˝∑÷±œýµ»£©£¨‘Úa°¢b”¶¬˙◊„µƒπÿœµ « £®”√∫¨a°¢bµƒ ˝—ß Ω±Ì æ£©°£
£®¢Ú£©ƒ≥–°◊È‘À”√𧓵…œ¿Î◊”Ωªªªƒ§∑®÷∆…’ºÓµƒ‘≠¿Ì£¨”√»Áœ¬ÕºÀ˘ æ◊∞÷√µÁΩ‚K2SO4»Ð“∫°£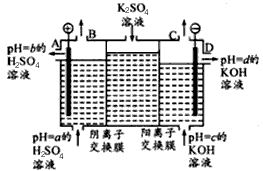
¢Ÿ∏√µÁΩ‚≤€÷–Õ®π˝“ı¿Î◊”Ωªªªƒ§µƒ¿Î◊” ˝ £®ÃÓ°∞>°±°∞<°±ªÚ°∞“ª°±£©Õ®π˝—Ù¿Î◊”Ωªªªƒ§µƒ¿Î◊” ˝£ª
¢⁄Õº÷–a°¢b°¢c°¢d∑÷±±Ì æ”–πÿ»Ð“∫µƒpH£¨‘Úa°¢b°¢c°¢d”…–°µΩ¥ÛµƒÀ≥–ÚŒ™ £ª
¢€µÁΩ‚“ª∂Œ ±º‰∫Û£¨B≥ˆø⁄”ÎC≥ˆø⁄≤˙…˙∆¯Ãµƒ÷ ¡ø±»Œ™ °£
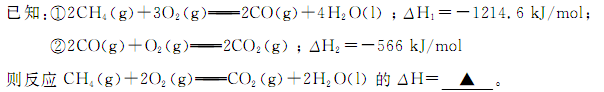
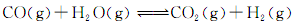 £¨µ√µΩ»Áœ¬»˝◊È ˝æð£∫
£¨µ√µΩ»Áœ¬»˝◊È ˝æð£∫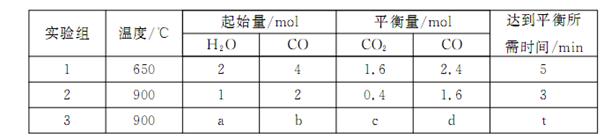

| ||
| °˜ |
| 1 |
| 2 |
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com